题目内容
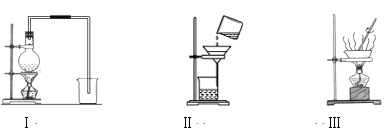
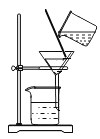
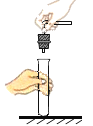
【题目】下图是实验室常见气体制备、净化、干燥、收集装置。某化学小组的同学欲利用其进行下列化学实验。

(1)装置A用于实验室制备O2,化学方程式为____________。
(2)装置B用于制取氢气,并进行氢气的可燃性实验。
①制取氢气的化学方程式为______________。
②用F收集氢气,气体应从______________端进入(填“f ”或“g”)。
③做氢气的可燃性试验时,点燃氢气前,一定要_______________。
(3)装置C用于制取CO2,并除去CO2中可能混有的水蒸气和HCl,以收集纯净干燥的CO2气体。从左到右正确的连接顺序为(填字母“ b”、“c”、“d”或“e”):(a)接(_______)→(_______)接(_______)→(_______)接(f)。E中所盛试剂除Na2CO3溶液外,还可用下列中的__________(填字母)。
A碳酸氢钠溶液 BNaOH溶液 C澄清石灰水 D石灰石
【答案】2H2O2![]() 2H2O+ O2↑ Zn + H2SO4 = ZnSO4 + H2 ↑ g 先检验氢气的纯度 d e b c A
2H2O+ O2↑ Zn + H2SO4 = ZnSO4 + H2 ↑ g 先检验氢气的纯度 d e b c A
【解析】
(1)固液发生装置A(不需要加热)用于实验室制备O2,过氧化氢溶液与二氧化锰混合反应产生水和氧气的化学方程式为2H2O2![]() 2H2O+ O2↑。
2H2O+ O2↑。
(2)装置B用于制取氢气,并进行氢气的可燃性实验。
①锌粒与稀硫酸反应产生硫酸锌和氢气的化学方程式为: Zn + H2SO4 = ZnSO4 + H2 ↑。
②氢气的密度小于空气,用万能瓶F收集氢气,气体应“短管进、长管出”从g端进入。
③氢气具有可燃性,做氢气的可燃性试验时,点燃氢气前,一定要:先检验氢气的纯度,防止发生危险。
(3)装置C用于制取CO2,并除去CO2中可能混有的水蒸气和HCl,以收集纯净干燥的CO2气体。应该先除杂,后干燥,所以先通入碳酸钠溶液除去氯化氢气体,再通入浓硫酸干杂二氧化碳气体;从左到右正确的连接顺序为:(a)接(d)→(e)接(b)→(c)接(f)。E中所盛试剂除Na2CO3溶液外,还可用下列中的:
A、碳酸氢钠溶液能与氯化氢反应产生二氧化碳气体,可以用于除杂;故选项正确;
B、NaOH溶液能与二氧化碳气体反应产生碳酸钠,不能用于除杂;故选项错误;
C、澄清石灰水能与二氧化碳反应产生碳酸钙沉淀,不能用于除杂;故选项错误;
D、E中所盛试剂应是液体,石灰石固体,不能用于除杂;故选项错误;
故选:A。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】某兴趣小组在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液逐滴加入稀硫酸,一会儿发现忘记了滴加指示剂。此时,他们停止滴加稀硫酸,并对烧杯内溶液中的溶质成分进行探究。
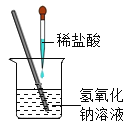
(1)写出该中和反应的化学方程式为______________;
(2)探究烧杯内溶液中溶质的成分:
(提出问题)该烧杯内溶液中的溶质是什么?
(猜想)猜想一:溶质有硫酸钠和氢氧化钠;猜想二:溶质只有硫酸钠;猜想三:_________;
(进行实验)
实验步骤 | 可能观察到的现象 | 结 论 |
①取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡; | _______________ | 猜想一不正确 |
②再取少量烧杯内溶液于另一支试管中,逐滴加入_____溶液至过量 | ______________ | 猜想二不正确,猜想三正确。 |
(反思与拓展)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑__________;