题目内容
某化学兴趣小组的同学对食品保鲜袋进行了如下研究.【研究课题】食品保鲜袋的元素组成.
【查阅资料】碱石灰是由NaOH和CaO组成的吸湿剂;无水硫酸铜可作吸水剂,且吸水后由白色变为蓝色.
【提出猜想】保鲜袋可能由“碳、氢、氧”中的两种或三种元素组成.
【实验设计】小组同学设计了如下实验装置,利用燃烧法测定保鲜袋的元素组成.
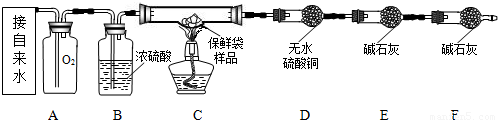
【实验步骤】
(1)按上图图示连接好仪器.
(2)检查装置的气密性.
(3)按图示装好药品和1.4g剪碎的保鲜袋样品,除D、E、F外将仪器按原图组装.
(4)向A中缓慢注水一段时间后,将已称重的D、E两干燥管和未称重的F干燥管接到C的尾端.
(5)点燃C处的酒精灯,直至保鲜袋子碎片完全燃烧.
(6)熄灭酒精灯并继续向A中注水一段时间.
(7)分别对D、E进行第2次称重.
【实验分析】
(1)B处的浓硫酸的作用是.F处干燥管的作用是.
(2)在点燃酒精灯前,要向A中缓慢注水一段时间是为了.
(3)熄灭酒精灯后继续向A中注水一段时间是为了.
(实验结论)第1次对D、E称重质量分别为54.2g、48.0g;第2次对D、E称重质量分别为56.0g、52.4g,则该食品保鲜袋的元素组成为.
【答案】分析:本题为物质成分的探究题,为保证实验结果的客观准确性,需要排除某些物质对实验的干扰,浓硫酸具有吸水性,能用作干燥剂,点燃酒精灯前向A注水是为了将装置中的空气排尽,碱石灰起到吸收空气中的水和二氧化碳的作用,防止进入E装置,熄灭酒精灯继续向A注水是为了将产生的气体全部吸收,DE装置质量增加,说明生成了水和二氧化碳,故该包装袋含有碳元素和氢元素.
解答:解:(1)浓硫酸具有吸水性,能用作干燥剂,碱石灰起到吸收空气中的水和二氧化碳的作用,防止进入E装置,影响实验结果;所以本题答案为:吸收水分,防止空气中的水分和CO2进入E装置;
(2)点燃酒精灯前向A注水是为了将装置中的空气排尽,并将氧气充入到C中,所以本题答案为:排出玻璃管C中的空气,将足量的氧气充入到C装置中,确保样品完全燃烧;
(3)熄灭酒精灯继续向A注水是为了将产生的气体全部吸收,D装置质量增加,说明生成了水,E装置质量增加,说明生成了二氧化碳,故该包装袋一定含有碳元素和氢元素,D增重的量为56.0g-54.2g=1.8g,所含氢元素的质量为:1.8g× =0.2g,E增重的量为52.4g-48g=4.4g,所含碳元素的质量为:4.4g×
=0.2g,E增重的量为52.4g-48g=4.4g,所含碳元素的质量为:4.4g×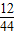 =1.2g,所以m氢+m碳=0.2g+1.2g=1.4g,故该物质中一定不含氧元素,所以本题答案为:使C中的水蒸气及CO2气体完全被D、E装置吸收,碳元素和氢元素.
=1.2g,所以m氢+m碳=0.2g+1.2g=1.4g,故该物质中一定不含氧元素,所以本题答案为:使C中的水蒸气及CO2气体完全被D、E装置吸收,碳元素和氢元素.
点评:本题考查了物质组成成分的实验探究,完成此题,可以依据题干提供的信息,结合已有的知识进行,要求同学们能够对所学的知识进行灵活应用.
解答:解:(1)浓硫酸具有吸水性,能用作干燥剂,碱石灰起到吸收空气中的水和二氧化碳的作用,防止进入E装置,影响实验结果;所以本题答案为:吸收水分,防止空气中的水分和CO2进入E装置;
(2)点燃酒精灯前向A注水是为了将装置中的空气排尽,并将氧气充入到C中,所以本题答案为:排出玻璃管C中的空气,将足量的氧气充入到C装置中,确保样品完全燃烧;
(3)熄灭酒精灯继续向A注水是为了将产生的气体全部吸收,D装置质量增加,说明生成了水,E装置质量增加,说明生成了二氧化碳,故该包装袋一定含有碳元素和氢元素,D增重的量为56.0g-54.2g=1.8g,所含氢元素的质量为:1.8g×
 =0.2g,E增重的量为52.4g-48g=4.4g,所含碳元素的质量为:4.4g×
=0.2g,E增重的量为52.4g-48g=4.4g,所含碳元素的质量为:4.4g×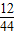 =1.2g,所以m氢+m碳=0.2g+1.2g=1.4g,故该物质中一定不含氧元素,所以本题答案为:使C中的水蒸气及CO2气体完全被D、E装置吸收,碳元素和氢元素.
=1.2g,所以m氢+m碳=0.2g+1.2g=1.4g,故该物质中一定不含氧元素,所以本题答案为:使C中的水蒸气及CO2气体完全被D、E装置吸收,碳元素和氢元素.点评:本题考查了物质组成成分的实验探究,完成此题,可以依据题干提供的信息,结合已有的知识进行,要求同学们能够对所学的知识进行灵活应用.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
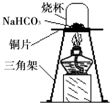 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.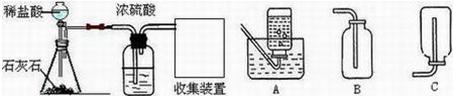
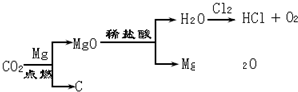
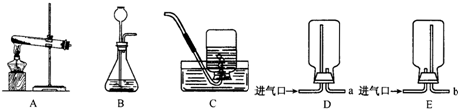
 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.