题目内容
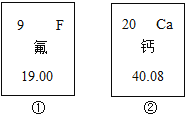
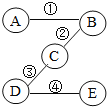
【题目】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。
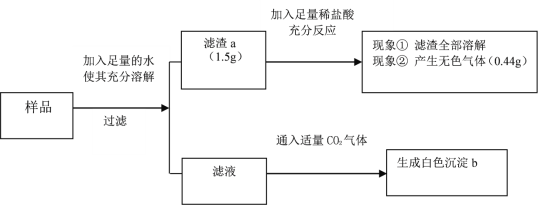
请回答下列问题:
(1)过滤操作中玻璃棒的作用是____________;
(2)加入足量的稀盐酸,滤渣a全部溶解的化学方程式为_________(若有多个反应,写出一个即可);
(3)样品中一定不含有的物质是___________(写名称或化学式均可,下同),滤液中溶质是__________;
(4)若现象① “滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品中不能确定是否存在的物质是___________。
【答案】引流 CaCO3+2HCl =CaCl2+H2O+CO2↑;Mg(OH)2+2HCl=MgCl2+2H2O 硫酸钠 氢氧化钠、氯化钠和氯化钡 氯化镁
【解析】
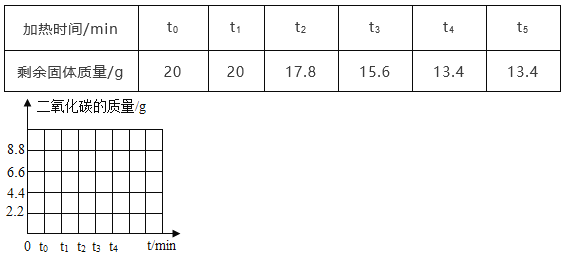
滤渣a能全部与稀盐酸反应,故说明滤渣中不含有硫酸钡沉淀,故原混合物中不能碳酸含有硫酸钠和氯化钡;设产生0.44g的二氧化碳需要碳酸钙的质量为x
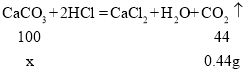
![]() ,故x=1.0g,1.0g小于1.5g,故说明滤渣中还含有氢氧化镁沉淀,故说明原混合物中一定含有碳酸钙、氯化镁、氢氧化钠。
,故x=1.0g,1.0g小于1.5g,故说明滤渣中还含有氢氧化镁沉淀,故说明原混合物中一定含有碳酸钙、氯化镁、氢氧化钠。
(1)过滤操作中的玻璃棒的作用是引流。
(2)加入足量的稀盐酸,稀盐酸与碳酸钙反应生成氯化钙、二氧化碳和水,反应方程式为:CaCO3+2HCl =CaCl2+H2O+CO2↑;稀盐酸与氢氧化镁反应生成氯化镁和水,反应方程式为;Mg(OH)2+2HCl=MgCl2+2H2O。
(3)向滤液中通入二氧化碳有白色沉淀生成,则滤液中含有氢氧化钠,与二氧化碳反应生成碳酸钠,碳酸钠与氯化钡反应生成白色沉淀,故不可能有硫酸钠,故滤液中含有氢氧化钠、氯化钠和氯化钡。
(4)若现象① “滤渣全部溶解”变为“滤渣部分溶解”,说明有碳酸钙沉淀和硫酸钡沉淀,不一定含有氢氧化镁沉淀,故不能确定是否含有氯化镁。

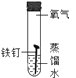
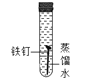
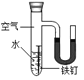
【题目】某同学为了探究铁钉生锈条件,设计了如下实验。
序号 | ① | ② | ③ | ④ |
实验内容 |
|
|
|
|
实验现象 | 铁钉无明显变化 | 铁钉生锈 | 铁钉无明显变化 | 铁钉生锈,U型管左侧液面上升,右侧液面下降 |
(1)通过实验①、②对比得出的结论是_____。
(2)增加实验③的目的是_____。
(3)实验④中,导致“U型管左侧液面上升,右侧液面下降”的原因是_____。