题目内容
【题目】下图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器,欲利用其进行下列化学实验。
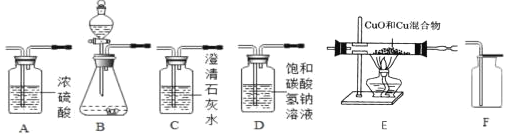
(1)以石灰石和稀盐酸为原料,在实验室中制备、收集干燥纯净的二氧化碳气体(提示:挥发出的少量 HCl 气体可用饱和碳酸氢钠溶液吸收)。
①所选装置的连接顺序为_____→_____→_____→_____(填写装置字母序号)。
②生成二氧化碳气体时,装置 B 中所发生反应的化学方程式为__________。
③下列有关二氧化碳的的说法正确的是_____(选填下列序号之一)。
A 将少量二氧化碳气体通入大量澄清石灰水中,溶液的质量会增大
B 将 CO2 气体通入澄清的石灰水中,石灰水的 pH 将增大
C 二氧化碳能够扑灭木材着火的根本原因是它既不能燃烧,也不支持燃烧
D 以石灰石和稀盐酸为原料制取二氧化碳的剩余液中常含有少量盐酸,欲检验盐酸的存在,可选用硝酸银溶液进行验证
(2)若以 H2O2 溶液为原料(以 MnO2 为催化剂)在实验室中制备干燥的氧气,并用来测定 CuO 和 Cu 的混合物样品中 Cu 的质量分数。装置的连接顺序为:B→A→E。
①装置 A 中浓硫酸的作用是_____________。
②生成氧气时,装置 B 中所发生反应的化学方程式为____________。
③欲通过测量反应前后 E 处大玻璃管质量的增加,来计算样品中 Cu 的含量。若反应前CuO 和 Cu 样品的质量为 m 克,反应后 E 处大玻璃管内固体质量增加 n 克,则样品中Cu 的质量分数为_______×100%。
④完成上述实验后,小波同学将 E 处大玻璃管内的剩余固体全部倒入烧杯中,并向烧杯中加入足量的稀硫酸,充分反应后发现,溶液变成_____色,溶液底部有少量红色的固体。样品中 Cu 的质量分数的测算结果与真实值相比将________(填“偏大”、“偏小”或“不受影响”之一)
【答案】B D A F ![]() C 干燥氧气(吸收氧气中的水分)
C 干燥氧气(吸收氧气中的水分) 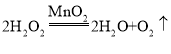
![]() 蓝 偏小
蓝 偏小
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙和水,过氧化氢在二氧化锰催化作用下生成水和氧气,铜和氧气加热生成氧化铜,稀硫酸和氧化铜反应生成硫酸铜和水。
(1)①碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应在常温下进行,选用固液常温型制取装置,二氧化碳中带有挥发出的少量 HCl 气体,用饱和碳酸氢钠溶液吸收,然后用浓硫酸干燥二氧化碳气体,二氧化碳密度比空气大,用向上排空气法收集,故所选装置的连接顺序为B→D→A→F。
②生成二氧化碳气体时,装置 B 中所发生反应是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为![]() 。
。
③A、将少量二氧化碳气体通入大量澄清石灰水中,二氧化碳和氢氧化钙反应生成碳酸钙和水,溶液的质量减小,故A不正确;
B、将 CO2 气体通入澄清的石灰水中生成碳酸钙和水,石灰水的 pH 将减小,故B不正确;
C、二氧化碳能够扑灭木材着火的根本原因是它既不能燃烧,也不支持燃烧,故C正确;
D、碳酸钙和稀盐酸反应生成氯化钙,氯化钙和盐酸均与硝酸银反应生成氯化银沉淀,欲检验盐酸的存在,不能选用硝酸银溶液进行验证,故D不正确。故选C。
(2)①浓硫酸具有吸水性,故装置 A 中浓硫酸的作用是干燥氧气(吸收氧气中的水分)。
②生成氧气时,装置 B 中所发生反应是过氧化氢在二氧化锰催化作用下生成水和氧气,反应的化学方程式为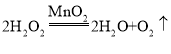 。
。
③铜和氧气加热生成氧化铜,反应后 E 处大玻璃管内固体质量增加 n 克,说明生成的氧气的质量为n克
设样品中 Cu 的质量为x
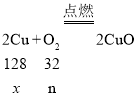
![]()
![]()
故样品中Cu 的质量分数为![]() ×100%。
×100%。
④E 处大玻璃管内的剩余固体是氧化铜,全部倒入烧杯中,并向烧杯中加入足量的稀硫酸,稀硫酸和氧化铜反应生成硫酸铜和水,故溶液变成蓝色,溶液底部有少量红色的固体,说明含有铜未被氧化,测定的氧气的质量偏小,计算得到的铜的质量偏小,故样品中 Cu 的质量分数的测算结果与真实值相比将偏小。

【题目】下列实验对应的两种方案设计均不正确的是
选项 | 实验目的 | 实验方案一 | 实验方案二 | ||||||||||||
A | 鉴别碳酸氢钠和碳酸钠两种无色溶液 | 分别取少量溶液分别滴加少量稀硫酸,观察是否有气泡冒出 | 分别取少量溶液,分别滴加几滴无色酚酞溶液,观察溶液是否变红 | ||||||||||||
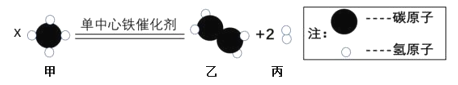
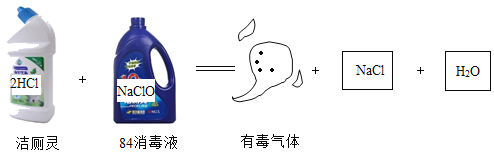
B | 一定条件下转化
|
|
| ||||||||||||
C | 区分硬水和软水 | 分别向等量水样中加入等量的肥皂水,振荡,观察泡沫的多少 | 分别取等量水样分别滴在玻璃片上,蒸发完毕后,水垢多的为硬水,反之为软水 | ||||||||||||
D | 除去氧气中混有的二氧化碳和水蒸气 | 通过氢氧化钠固体 | 依次通过氢氧化钠溶液和浓硫酸 |
A.AB.BC.CD.D