题目内容
【题目】(1)碘盐就是在食盐中加入一定量的碘酸钾(KIO3),回答下列问题.
碘酸钾的相对分子质量为_____;在碘酸钾中碘元素的质量分数是_____;_____ g 碘酸钾中含碘 25.4g。
(2)配制50g溶质的质量分数为4%的氢氧化钠溶液,需要氢氧化钠和水各多少克__________、__________ ?若要完全中和这些溶液.需要溶质的质量分数为3.65%的稀盐酸多少克_____?
【答案】214 59.3% 42.8 2g 48g 50g
【解析】
相对分子质量是指化学式中所有元素的相对原子质量的总和,某元素的质量分数是指该元素的质量与化合物质量的比值,根据溶质质量分数可以进行有关的计算。
(1)①碘酸钾的相对分子质量为:39+127+16×3=214,
碘元素的质量分数为:![]() ,
,
设碘酸钾的质量为x,
x×59.3%=25.4g
x=42.8,
②解:需要氢氧化钠的质量为:
50g×4%=2g
需要水的质量为:
50g﹣2g=48g
设:需要溶质的质量分数为3.65%的稀盐酸的质量为 y
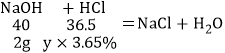
![]()
y=50g
答:需要氢氧化钠的质量为2g,需要水的质量为48g,需要盐酸的质量为50g.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
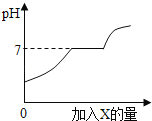
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
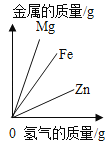
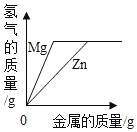
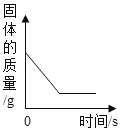
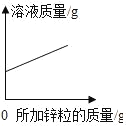
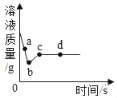
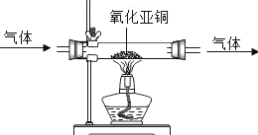
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D