题目内容
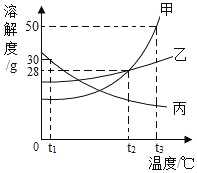
【题目】向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法不正确的是( )
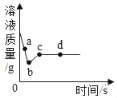
A. 取a点溶液,滴加稀盐酸,有白色沉淀出现
B. 图标上b~c段质量增加的原因是Zn和Cu(NO3)2溶液反应
C. b点时溶液中金属离子有Zn2+、Cu2+,金属单质只有Ag
D. c点和d点溶质种类不同,金属单质种类也不同
【答案】CD
【解析】
在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,与两种溶质依次发生反应
![]()
所以析出银的过程是溶液质量减少的过程;
![]()
所以析出铜的过程是溶液质量增加的过程
A、在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银,滴加稀盐酸,会生成白色沉淀,故A正确;
B、图标上b~c段表示锌和硝酸铜反应生成硝酸锌和铜,溶液质量增加,故B正确;
C、b点时表示锌与硝酸银恰好完全反应,金属单质中含金属单质Ag和未反应的Zn,因为此时溶液中含金属离子Zn2+、Cu2+,故C错误;
D、c点和d点表示锌和硝酸铜完全反应,所以溶质种类相同(只有硝酸锌),金属单质种类也相同(都为银、铜和过量的锌),故D错误。
故选:CD。

【题目】室验室开放日,小明、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,同学们决定对“固体与液体”之间的反应进行一系列探究.
(1)小明同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即产生了一种无色气体,对气体是何物质,同学们进行了大胆的猜想,小佳同学的猜想可能是①__________;②__________;….
(2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如下:
实验步骤 | 现象及结论 |
______________ | ______________ |
(3)小华想用如图给定的收集装置收集一瓶小佳同学猜想②中的气体,则气体由______________(填a或b)端进入.

(4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,但无气泡放出.同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面进行了大胆的猜想:
猜想一:______________;
猜想二:______________;
猜想三:______________;….