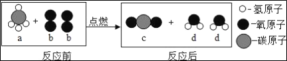
题目内容
【题目】Cu可以形成化合价为+2和+1的化合物,其中+l价化合物称为亚铜化合物。
(1)高温时,氧化铜可被木炭还原为铜,反应的化学方程式是_____,该反应属于基本反应类型中的_____反应。
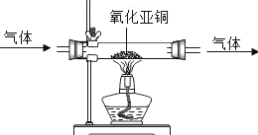
(2)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式是_____;利用这一性质可检验氮气中是否含有氧气(装置如图所示),判断氮气中含有氧气的现象是_____。
(3)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3还是Cu2O或是二者混合物。探究过程如下:
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO;
②Fe3+遇到KSCN试剂变红。
[提出假设]假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;
假设3:_____。
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
①若假设1成立,则实验现象是_____;
②若假设2成立,写出反应的化学方程式:_____。
[探究延伸]若经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物。实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为_____%。
【答案】2CuO+C![]() 2Cu+CO2↑ 置换 2Cu2O+O2
2Cu+CO2↑ 置换 2Cu2O+O2![]() 4CuO 红色粉末变成黑色 红色粉末是Cu2O和Fe2O3的混合物 红色固体溶解,溶液变成黄色,加入KSCN试剂后溶液变红 Cu2O+H2SO4=CuSO4+Cu+H2O
4CuO 红色粉末变成黑色 红色粉末是Cu2O和Fe2O3的混合物 红色固体溶解,溶液变成黄色,加入KSCN试剂后溶液变红 Cu2O+H2SO4=CuSO4+Cu+H2O ![]() %
%
【解析】
高温条件下氧化铜和碳反应生成铜和二氧化碳;
加热条件下氧化亚铜和氧气反应生成氧化铜;
氧化亚铜和稀硫酸反应生成硫酸铜、铜和水。
解析:(1)高温时,氧化铜可被木炭还原为铜,同时生成二氧化碳,反应的化学方程式是:2CuO+C![]() 2Cu+CO2↑,该反应属于基本反应类型中的置换反应。
2Cu+CO2↑,该反应属于基本反应类型中的置换反应。
故填:2CuO+C![]() 2Cu+CO2↑;置换。
2Cu+CO2↑;置换。
(2)加热时,氧化亚铜能与氧气发生化合反应生成氧化铜,反应的化学方程式是:2Cu2O+O2![]() 4CuO;
4CuO;
加热条件下氧化亚铜和氧气反应生成黑色固体氧化铜,判断氮气中含有氧气的现象是:红色粉末变成黑色。
故填:2Cu2O+O2![]() 4CuO;红色粉末变成黑色。
4CuO;红色粉末变成黑色。
(3)[提出假设]
假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;
假设3:红色粉末是Cu2O和Fe2O3的混合物。
故填:红色粉末是Cu2O和Fe2O3的混合物。
[设计探究实验]
①若假设1成立,氧化铁和稀硫酸反应生成硫酸铁和水,则实验现象是:红色固体溶解,溶液变成黄色,加入KSCN试剂后溶液变红。
故填:红色固体溶解,溶液变成黄色,加入KSCN试剂后溶液变红。
②若假设2成立,氧化亚铜和稀硫酸反应生成硫酸铜、铜和水,反应的化学方程式为:Cu2O+H2SO4=CuSO4+Cu+H2O。
故填:Cu2O+H2SO4=CuSO4+Cu+H2O。
[探究延伸]
设氧化亚铜质量为x,
反应的氧气质量为:bg﹣ag

x=9(bg﹣ag),
则混合物中Cu2O的质量分数为:![]() ×100%=
×100%=![]() %,
%,
故填:![]() 。
。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】(1)填写化学符号或化学符号表示的意义。
化学符号 | 2Fe | ________ |
| _____ |
表示意义 | __ | 三个氧分子 | 核内有____个质子 | 一个镁离子 |
(2)从C、S、H、O、N六种元素中选择适当的元素按要求填空。写出符合下列要求的物质的化学式:
①能用于人工降雨的是___; ②充入食品包装袋中可防腐的单质___;③能形成酸雨的空气污染物___;
④属于化石燃料的是_____。