��Ŀ����
����Ŀ��A��B��C��D��E��F�dz��л�ѧ�������������ʣ���֪A��һ�ֵ��ʣ� C��D��E�����ᡢ����е�һ�֣�BΪ�������Ҫ�ɷ֣� D�����ڸ�������������F��B����ͬ�����ʣ������Ӧ�������ͼ��ʾ�����ߡ�һ�����������ʼ��ܷ�Ӧ����ͷ��������ʾ�����ɣ���
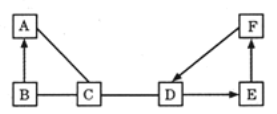
��1��A�Ļ�ѧʽΪ_____________��
��2��B��C�ķ�Ӧ����________________��Ӧ���������Ӧ���ͣ���
��3������F��������_____________����ᡢ��λ������
��4��д��C��D�Ļ�ѧ����ʽ_______
���𰸡�Fe ���ֽ� ������ Ca(OH)2��2HCl=CaCl2��2H2O
��������
BΪ�������Ҫ�ɷ֣���B��������������D�����ڸ���������������D�������������ƣ������������ɵ���A ,��A����������C����������Ӧ����������������Ӧ����C�������ᡢ����е�һ�֣���C�������ᣬ��������������E����E�Ǽ���е�һ�֣���E��̼��ƣ�F�������ƣ������飬����������
��1���ɷ�����֪��A��������ѧʽΪ��Fe��
��2�����������ᷴӦ���ڸ��ֽⷴӦ��
��3������F�������ƣ����������
��4������������ϡ���ᷴӦ�����Ȼ��ƺ�ˮ����Ӧ�ķ���ʽΪ��Ca(OH)2��2HCl=CaCl2��2H2O��

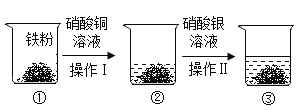
����Ŀ���Կ�ȸʯΪԭ����ȡ������CuSO45H2O���IJ��ֹ���������ͼ��ʾ��
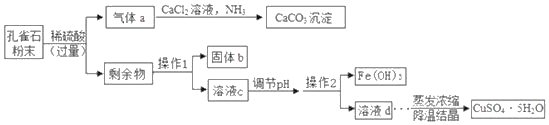
���������ϣ�
I����ȸʯ��Ҫ�ɷ�ΪCu2��OH��2CO3����������SiO2��������ˮ������ϡ���ᷴӦ����Fe2O3�����ʡ�
������һ����ɫ���壬�����ֽ⡣
���ڸ�ʵ�������£�Fe��OH��3��Cu��OHI��2������pH���±���
Fe��OH��3 | Cu��OH��2 | |
��ʼ������pH | 1.14 | 4.2 |
��ȫ������pH | 3.0 | 6.7 |
��1������1������Ϊ_____��ʵ���ҽ��иò���ʱ��������������_____��
��2������a����CaCO3��ͬʱ������NH4C1���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��3����Һc�е������У�CuSO4��H2SO4��_____��д��ѧʽ��
��4��Ϊ����Һ�е�Fe3+ȫ��ת��ΪFe��OH��3��������Cu2+��ת��ΪCu��OH��2������Ӧ����pH��m��m�ķ�Χ��_____��
��5����õ�������ʱ���ý��½ᾧ�����������ᾧ����Ҫԭ����_____��