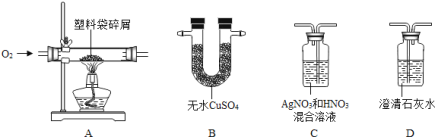题目内容
【题目】某同学用如图所示的装置测定空气中氧气的含量,对实验认识正确的是( )

A. 选用红磷是因为反应可以消耗氧气,生成固体
B. 将红磷可以改为铁丝、蜡烛
C. 实验中红磷量越多,水位上升越高
D. 本实验可以证明空气中约含有氮气78%、氧气21%,其它气体和杂质1%
【答案】A
【解析】测定空气中氧气含量实验的实验原理是在密闭容器内消耗氧气,测量容器内气体体积的减少量确定氧气的含量.因此在选择消耗氧气的药品时,应考虑能与空气中的氧气反应而不与空气中的其他成分反应,生成物是固体不能为气体;还应注意装置不漏气,药品的量要足,读数时温度要冷却至室温等.
解:A,因红磷能与空气中的氧气反应生成固态,故A正确;
B,因铁丝在空气中不能燃烧,因此红磷不能用铁丝代替;蜡烛与氧气反应生成二氧化碳气体,因此也不能用蜡烛代替,故B不正确;
C,红磷的量足,能耗尽氧气,因此实验中红磷足量即可,并不是越多,水位上升越高,因此C不正确;
D,该实验中红磷只与空气中氧气反应,所以只能确定空气中有氧气,剩余气体的成分不能确定,因此D不正确.
故选A.

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组的同学采用了下图所示装置测定空气中氧气含量。
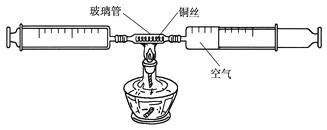
在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是__________________;
(2)写出该实验过程中玻璃管内的现象为_______________________________,写出该反应的符号表达式________________________________;
(3)小强实验操作均正确,测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 20mL |
该实验得出的结论为 ____________________________________;
小红同学实验误差较大,请你帮她分析造成误差的原因_____________(写出一条即可)。