题目内容
(2012?滨湖区二模)将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体.某研究性学习小组对蓝色固体的成分进行了如下探究.请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由:
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈
猜想三:固体为Cu(OH)2和CuCO3的混合物.
(二)资料查阅:
(1)Cu(OH)2和CuCO3晶体均不带结晶水;
(2)Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物.
(3)无水硫酸铜为白色,吸水后会变成蓝色.
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经
(2)判断固体已洗净的方法及现象
Ⅱ.用如图所示装置,定性探究固体的成分.

(3)若用装置A、B组合进行实验,B中无现象,则猜想二正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想一正确;
(5)小组同学将装置按 A、
结论:固体为Cu(OH)2和CuCO3的混合物.
Ⅲ.固体成分定量测定:
(6)小组同学称取该固体样品20 g,逐滴加入稀盐酸至无气泡冒出为止,共用去稀盐酸100克,所得溶液质量为115.6克,请计算该固体样品中CuCO3的质量分数.
(一)猜想与假设:
猜想一:固体为CuCO3,理由:
Na2CO3+CuSO4═CuCO3↓+Na2SO4
Na2CO3+CuSO4═CuCO3↓+Na2SO4
(用化学反应方程式表示).猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈
碱
碱
(填“酸”或“碱”)性.猜想三:固体为Cu(OH)2和CuCO3的混合物.
(二)资料查阅:
(1)Cu(OH)2和CuCO3晶体均不带结晶水;
(2)Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物.
(3)无水硫酸铜为白色,吸水后会变成蓝色.
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经
过滤
过滤
、洗涤、低温烘干得蓝色固体.(2)判断固体已洗净的方法及现象
取最后洗涤液少量于试管中,滴加适量的稀盐酸(硝酸、硫酸),无气泡产生
取最后洗涤液少量于试管中,滴加适量的稀盐酸(硝酸、硫酸),无气泡产生
.Ⅱ.用如图所示装置,定性探究固体的成分.

(3)若用装置A、B组合进行实验,B中无现象,则猜想二正确;
(4)若用装置A、C组合进行实验,C中无现象,则猜想一正确;
(5)小组同学将装置按 A、
C、B
C、B
(填“B、C”或“C、B”)的顺序组合进行实验,验证出猜想三是正确的,实验中:B中的现象为石灰水变浑浊
石灰水变浑浊
,C中的现象为白色固体变蓝
白色固体变蓝
.结论:固体为Cu(OH)2和CuCO3的混合物.
Ⅲ.固体成分定量测定:
(6)小组同学称取该固体样品20 g,逐滴加入稀盐酸至无气泡冒出为止,共用去稀盐酸100克,所得溶液质量为115.6克,请计算该固体样品中CuCO3的质量分数.
分析:【猜想与假设】猜想一:根据碳酸钠和硫酸铜反应生成蓝色沉淀进行分析;
猜想二:根据氢氧根离子会与铜离子生成氢氧化铜沉淀进行分析;
【设计与实验】(1)根据将固体和液体进行分离的方法进行分析;
(2)根据澄清石灰水会与二氧化碳反应检验二氧化碳的存在进行分析;
(5)要分析检验水和二氧化碳的顺序;
(6)根据质量减少为二氧化碳的质量求出碳酸铜的质量进而求出CuCO3的质量分数进行解答.
猜想二:根据氢氧根离子会与铜离子生成氢氧化铜沉淀进行分析;
【设计与实验】(1)根据将固体和液体进行分离的方法进行分析;
(2)根据澄清石灰水会与二氧化碳反应检验二氧化碳的存在进行分析;
(5)要分析检验水和二氧化碳的顺序;
(6)根据质量减少为二氧化碳的质量求出碳酸铜的质量进而求出CuCO3的质量分数进行解答.
解答:解:【猜想与假设】猜想一:碳酸钠和硫酸铜反应生成碳酸铜沉淀和硫酸钠,化学反应方程式为:Na2CO3+CuSO4=CuCO3↓+Na2SO4;
猜想二:碳酸钠是强碱弱酸盐,在水中会进行水解生成氢氧根离子,显碱性;
【设计与实验】(1)过滤是将不溶性物质从溶液中分离的一种操作,该题需要将固、液分离,操作为:过滤;
(2)固体上残留的碳酸钠会与盐酸反应生成二氧化碳气体,判断固体已洗净的方法及现象为:取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3)B中无明显现象,说明了没有二氧化碳生成,固体中也就没有碳酸铜,故答案为:二;
(4)C中无明显现象,说明没有水生成,固体中也就没有氢氧化铜,故答案为:一;
(5 )要证明生成物中有水和二氧化碳,应先证明水再证明二氧化碳,将装置按 A、C、B的顺序安装;实验中:B中的现象为石灰水变浑浊;C中的现象为白色固体变蓝,说明固体为Cu(OH)2和CuCO3的混合物;
(6)设碳酸铜的质量为x.
二氧化碳的质量为20g+100g-115.6g=4.4g
CuCO3+2HCl=CuCl2+H2O+CO2↑
124 44
x 4.4g
=
x=12.4g
该固体样品中CuCO3的质量分数=
×100%=62%
答:该固体样品中CuCO3的质量分数62%.
故答案为:猜想一:Na2CO3+CuSO4═CuCO3↓+Na2SO4;
猜想二:碱;
(三)设计与实验:
(1)过滤;
(2)取最后洗涤液少量于试管中,滴加适量的稀盐酸,无气泡产生;
(5)C、B;石灰水变浑浊;白色固体变蓝;
(6)62%.
猜想二:碳酸钠是强碱弱酸盐,在水中会进行水解生成氢氧根离子,显碱性;
【设计与实验】(1)过滤是将不溶性物质从溶液中分离的一种操作,该题需要将固、液分离,操作为:过滤;
(2)固体上残留的碳酸钠会与盐酸反应生成二氧化碳气体,判断固体已洗净的方法及现象为:取最后洗涤液少量,滴加适量的稀盐酸,无气泡产生;
(3)B中无明显现象,说明了没有二氧化碳生成,固体中也就没有碳酸铜,故答案为:二;
(4)C中无明显现象,说明没有水生成,固体中也就没有氢氧化铜,故答案为:一;
(5 )要证明生成物中有水和二氧化碳,应先证明水再证明二氧化碳,将装置按 A、C、B的顺序安装;实验中:B中的现象为石灰水变浑浊;C中的现象为白色固体变蓝,说明固体为Cu(OH)2和CuCO3的混合物;
(6)设碳酸铜的质量为x.
二氧化碳的质量为20g+100g-115.6g=4.4g
CuCO3+2HCl=CuCl2+H2O+CO2↑
124 44
x 4.4g
| 124 |
| x |
| 44 |
| 4.4g |
x=12.4g
该固体样品中CuCO3的质量分数=
| 12.4g |
| 20g |
答:该固体样品中CuCO3的质量分数62%.
故答案为:猜想一:Na2CO3+CuSO4═CuCO3↓+Na2SO4;
猜想二:碱;
(三)设计与实验:
(1)过滤;
(2)取最后洗涤液少量于试管中,滴加适量的稀盐酸,无气泡产生;
(5)C、B;石灰水变浑浊;白色固体变蓝;
(6)62%.
点评:通过该题,需要掌握检验混合物中的水蒸汽和二氧化碳时,应先检验水蒸汽,再检验二氧化碳,因为若先检验二氧化碳的话,即使原混合物中没有水蒸汽也会从石灰水中带出水蒸汽.除去混合物中的水蒸汽和二氧李碳时,应先除二氧化碳,再除水蒸汽,因为若先除水蒸汽的话,通过石灰水或氢氧化钠溶液除二氧化碳时又会让气体中混入水蒸汽.

练习册系列答案
相关题目
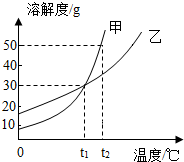 (2012?滨湖区二模)甲、乙两物质的溶解度曲线如图所示,下列叙述正确的是( )
(2012?滨湖区二模)甲、乙两物质的溶解度曲线如图所示,下列叙述正确的是( )