题目内容
【题目】化学小组为探究铁、铜、锌、银的金属活动性顺序,设计如下三个实验(其中金属均已打磨,其形状、大小及同种稀盐酸的用量均相同):
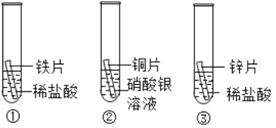
(1)实验①的化学方程式为______;一段时间后,观察到实验②的铜片表面有银白色固体附着,这说明铜比银的活动性______(填“强”或“弱”)。
(2)甲同学认为通过实验①和③可比较锌和铁的金属活动性,他依据的实验现象是______。
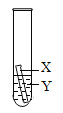
(3)乙同学认为上述实验方案不足以得出四种金属的活动性顺序,并在上述实验的基础上补充了一个实验(如图所示),实现了探究目的,则乙同学的实验:X是金属______,Y是______溶液。
【答案】![]() 强 锌表面产生气泡快,铁表面产生气泡慢 Fe(或Cu) CuSO4(或HCl)
强 锌表面产生气泡快,铁表面产生气泡慢 Fe(或Cu) CuSO4(或HCl)
【解析】
上述三个试管中都会发生化学反应,并由此可证明锌>铁>氢,铜>银,但铜与铁的活动性强弱不能证明,因此要加一个实验来证明,可以直接用金属与盐溶液反应,也可通过与酸反应证明。
(1)铁排在氢的前面所以能与盐酸反应放出氢气,化学方程式为![]() ,铜比银活动性强,才能置换出银溶液中的银,铜片表面有银白色固体附着;
,铜比银活动性强,才能置换出银溶液中的银,铜片表面有银白色固体附着;
(2)排在氢前面的金属能与酸反应放出氢气并且金属越活泼与酸反应就越剧烈,产生的气泡就越快,锌>铁>氢,现象是锌表面产生气泡快,铁表面产生气泡慢;
(3)上述三个试管中发生的化学反应证明锌>铁>氢>,铜>银,但铜与铁的活动性强弱不能证明,可以直接用铁与硫酸铜溶液或者铜和稀盐酸或者铜和硫酸亚铁溶液证明等。

【题目】目前,废旧电池对环境的污染越来越引起人们的重视。为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池有效回收再利用技术。如图为普通电池(锌锰电池)示意图,请你根据图示
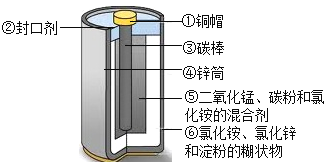
(1)将回收的废旧电池进行分离,可以得到的单质有______(用化学式表示,下同),氧化物有______,盐有______,有机物有______(写名称)。
(2)小李同学想得到⑤中纯净干燥的二氧化锰和氯化铵溶液,并检验氯化铵中的铵根离子。设计了如下实验步骤,请你帮他完成:
实验步骤 | 实验现象 | 结论或解释 |
①剥开干电池,取出碳棒周围的黑色粉末 | ||
②溶解、______(填操作名称)、洗涤 | 得到黑色粉末和无色澄清液体 | 黑色粉末的成分为______ |
③对黑色粉末进行______ | 得到纯净的 | |
④检验第②步中得到的无色澄清液体中是否含铵根离子的方法是:______ | ______ | 化学方程式为______ |