题目内容
【题目】(1)金属铁是由_____(填“原子”、“分子”或“离子”,下同)构成的,氯化钠是由_____构成的。
(2)原子得到或失去电子后形成离子。某离子的结构示意图为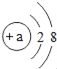
①当a=_____时,该粒子是原子。
②当a=8时,该粒子是_____(填“原子”、“阳离子”或“阴离子”)其符号为_____。
③当a=13时,该粒子是_____(填“原子”、“阳离子”或“阴离子”),其原子的最外层电子数是_____。
【答案】原子 离子 10 阴离子 O2- 阳离子 3
【解析】
(1)金属都是由离子构成的;氯化钠是由钠离子、氯离子两种离子构成的。
(2)①原子中质子数=核外电子数。②质子数<核外电子数的离子是阴离子。质子数为8的原子是氧原子,其最外层有6个电子,易得到两个电子,形成的氧离子带两个单位的负电荷,其离子符号是O2﹣。③质子数>核外电子数的离子是阳离子,质子数为13的原子是铝原子,铝原子的最外层有3个电子。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】溶液在日常生活和生产中应用广泛,请回答下列问题;
(1)糖水、生理盐水、白酒都是溶液。它们的共同点是:_________、_________、混合物。
(2)写出下列溶液中溶质的化学式:盐酸________、澄清石灰水________、碘酒________、
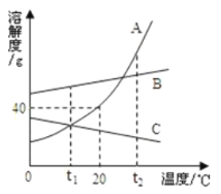
(3)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
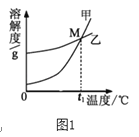
① 图1中能表示KNO3溶解度曲线的是_______(填“甲”或“乙”)。
② 若甲中混有少量的乙,最好采用__________方法提纯甲
(4)60℃时,向两个分别盛有相同质量的K2CO3和KNO3的烧杯中,各加入100g水,充分溶解后,恢复至60℃,其结果如图2所示。则烧杯①中的溶质是______,此时烧杯①溶液的溶质质量分数为_______。
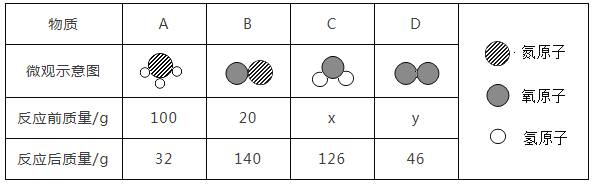
【题目】有关物质组成及化学规律的发现对化学的发展做出了重要贡献。
(1)法国化学家拉瓦锡为化学学科的发展做出了巨大贡献,下列有关发现与他有密切关系的是_____。
A. 空气的组成 B. 质量守恒定律 C. 水的组成 D. 酸碱指示剂
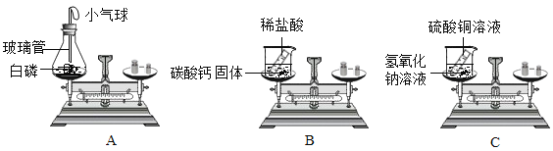
(2)在密闭容器内加入下列两种物质,并称量加入前后的总质量(含密闭容器),能验证质量守恒定律的是_____________(填标号)。
A. 蔗糖和水 B. 氯化钠溶液和硝酸钾溶液 C. 氯化钡溶液和稀硫酸
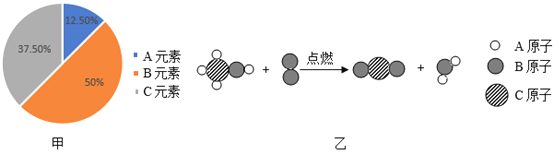
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。
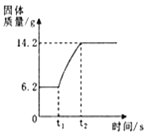
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是___________。
②该反应的化学方程式为________________。
③参加反应的氧气质量为___________g。
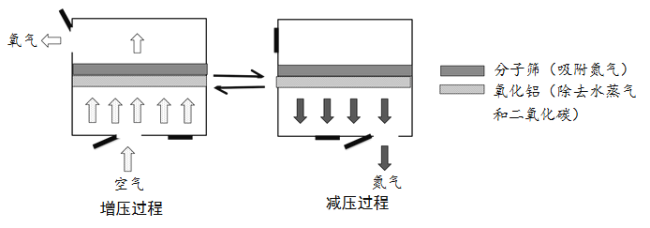
(4)某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。
查阅资料可知Mg、Mg3N2能发生如下反应:
①2Mg+O2 △ 2MgO; ②3Mg+N2 △ Mg3N2; ③2Mg+CO2 △ 2MgO+C
④Mg+H2O △ MgO+H2↑ ⑤Mg3N2+6H2O 3Mg(OH)2↓+2NH3↑
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题:
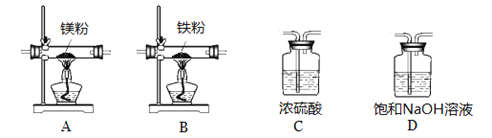
①连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是______(填装置序号)。D装置中发生反应的化学方程式为___________。
②通气后,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?_________。
③设计一个实验,验证产物是否含氮化镁:
实验操作和实验现象 | 实验结论 |
________________________ | 产物中含有氮化镁 |
④思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N的质量,请给出合理的解释_______________。