题目内容
如图所示,某Vc含片的包装。试求:
(1)Vc分子中原子个数比;
(2)相对分子质量;
(3)各元素的质量比;
(4)维生素 C中氧元素的质量分数;
(5)若每日服用 2片含片,即可满足每日摄入 500mg维生素的需要。则含片中Vc的含量为多少?
(1)C、H、O原子个数比为3:4:3 (2)176 (3)C:H:O=9:1:12 (4)54.6% (5)12.5%
解析试题分析:(1)化学式中右下角的数字(解码)表示化合物的一个分子中各原子的个数,故Vc分子中C、H、O三种原子的个数比=6:8:6=3:4:3;(2)Vc(C6H8O6)的相对分子质量=12×6+1×8+16×6=176;(3)Vc中碳、氢、氧元素的质量比=12×6: 1×8: 16×6=9:1:12;(4)Vc中氧元素的质量分数=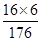 ×100%=54.6%;含片中Vc的含量=
×100%=54.6%;含片中Vc的含量=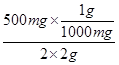 ×100%=12.5%。
×100%=12.5%。
考点:根据化学式的计算。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
为测定部分变质的氢氧化钠样品中变质的氢氧化钠的质量,某同学取该样品l3.3g于烧杯中,用滴管向其中慢慢滴加质量分数为7.3%的稀盐酸,当滴加稀盐酸lO0g,溶液中开始产生气泡,继续向其中滴加稀盐酸50g,恰好不再产生气泡,由此可知该样品中变质的氢氧化钠的质量是( )
| A.0.4g | B.0.8g | C.8g | D.4g |
在一个密闭容器内有如下反应,反应前后测得各物质的质量如下表所示:
| 物质 | M | N | P | Q |
| 反应前的质量/g | 40 | 4 | 3.6 | 4.8 |
| 反应后的质量/g | 待测[ | 13 | 12.6 | 10.8 |
A.该反应为化合反应 B.反应生成的P和Q的质量比为2︰3
C.待测值为16 D.N和P的相对分子质量之比为1︰1