题目内容
【题目】称取12.5g石灰石放人烧杯中,向其中加入50g稀盐酸,一者恰好完全反应(杂质不反应)。反应结束后称量烧杯中剩余物质的总质量为58.1g,请计算:①生成二氧化碳_____克。
②石灰石中碳酸钙的质量分数_____?
【答案】4.4 80%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算石灰石中碳酸钙的质量分数。
解:①根据质量守恒定律,二氧化碳的质量为:12.5g+50g-58.1g=4.4g;
②设该石灰石样品中碳酸钙的质量分数为x,
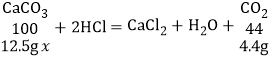
![]()
x=80%;
答:(1)生成的二氧化碳的质量为4.4g;
(2)石灰石中碳酸钙的质量分数为80%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
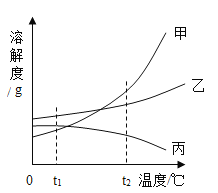
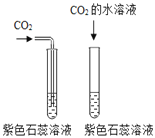
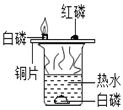
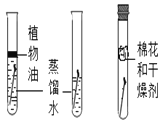
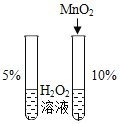
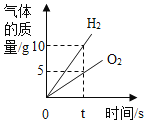
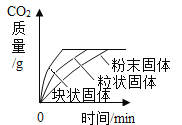
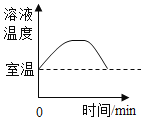
【题目】对比实验、控制变量是学习化学的重要方法,下列对比实验不能达到目的的是( )
编号 | A | B | C | D |
实验设计 |
|
|
|
|
实验目的 | 探究 | 探究物质燃烧的条件 | 探究生锈条件 | 探究 |
A. A B. B C. C D. D