题目内容
【题目】学会物质的分离提纯和准确配制一定质量分数的溶液在实际应用中有重要意义。(已知:20℃氧化钠的溶解度为36g,水的密度可近似看作1g/mL)。
实验一:溶液配制
(1)用氯化钠固体配制100g质量分数为6%的氯化钠溶液。需要氯化钠____________g。水__________mL。
(2)0.9%的医用氯化钠济液俗称生理盐水,可用于补充人体所需电解质。生理盐水中的溶质为____________。
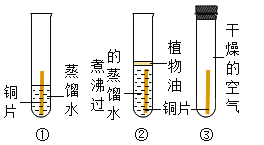
实验二:粗盐提纯
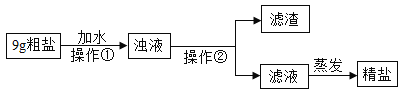
(3)操作①中玻璃棒的作用是___________,操作②的名称为_____________。
(4)20℃时提纯9g粗盐,若已知粗盐中氯化钠含量约为80%,溶解时应选择_____________的量筒量取所需要的水最为合适。(提供的量筒规格有“10mL ”“25mL”“50mL”和“100mL”)
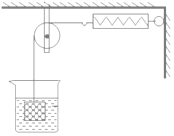
(5)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
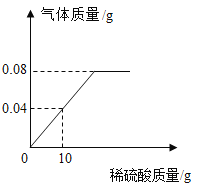
①铁粉反应完时,产生氢气的质量为____________g。
②原稀硫酸中溶质的质量分数(写出计算过程)。______
【答案】6g 94g 氯化钠 搅拌,加速溶解 过滤 25mL 0.08g 19.6%
【解析】
(1)100g质量分数为6%的氯化钠溶液中氯化钠的质量为:100g×6%=6g。故需要水的质量为:100g-6g=94g。
(2)生理盐水中的溶质是氯化钠。
(3)操作①是溶解,其中玻璃棒的作用是搅拌,加速溶解。操作2是将固体和液体分离的步骤,故是过滤。
(4)20℃时提纯9g粗盐,若已知粗盐中氧化钠含量约为80%,粗盐中氯化钠的质量为:9g×80%=7.2g,该温度下氯化钠的溶解度为36g,故完全溶解7.2g氯化钠需要水的质量为20g,就是20mL,因此需要25mL的量筒合适,故填:25mL;
(5)①由图可知, 完全反应后生成氢气的质量为0.08g。
②设生成0.04g氢气需要硫酸的质量为x
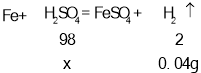
![]() 解得x=1.96g
解得x=1.96g
原稀硫酸中溶质的质量分数为:![]() ×100%=19.6%。
×100%=19.6%。