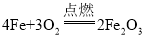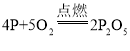题目内容
【题目】下列叙述不正确的是

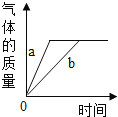
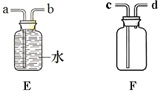
A. 如图关于水电解实验,若a试管气体为5 mL,则b试管气体为10 mL
B. 在水的电解实验中与电源负极相连的导管中产生氢气
C. 常用肥皂水检验硬水和软水
D. 用5%的过氧化氢溶液制氧气,为加快该反应的速率常加少量二氧化锰作催化剂
【答案】A
【解析】
A、由电解水的试验装置图可知,若a试管收集到的气体为5mL,该气体是电源的负极产生的气体是氢气,则b试管收集到的气体氧气,为2.5mL,故错误;
B、在水的电解实验中与电源负极相连的导管中产生氢气,正极是氧气,故正确;
C、检验硬水和软水的方法加肥皂水,泡沫少的是硬水,泡沫多的是软水,故正确;
D、用5%的过氧化氢溶液制氧气,为加快该反应的速率常加少量二氧化锰作催化剂,其催化作用,故正确。
故选A。

 阅读快车系列答案
阅读快车系列答案【题目】实验室用如图装置制取、干燥、收集气体正确的是( )
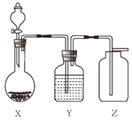
A | B | C | D | |
X | 过氧化氢溶液与 二氧化锰 | 锌粒与 稀硫酸 | 大理石与 稀盐酸 | 氯酸钾与 二氧化锰 |
Y | 浓硫酸 | 浓硫酸 | 氢氧化钠 | 浓硫酸 |
Z | O2 | H2 | CO2 | O2 |
A.AB.BC.CD.D
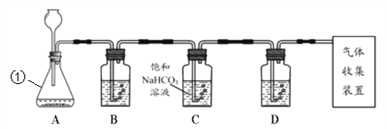
【题目】根据如图实验回答:
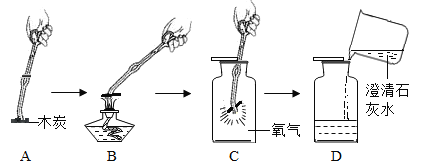
(1)写出实验中发生反应的化学方程式。(至少 写2个)_______、_______
(2)该实验探究的目的是什么?并说明对应的现象。(至少2条)_______、_______
【题目】下列表述不正确的是( )
选项 | 反应物及反应条件 | 反应化学方程式 | 实验现象 |
A | 铁丝在氧气中燃烧 |
| 剧烈燃烧,火星四射,生成黑色固体 |
B | 磷在空气中燃烧 |
| 产生大量白烟,放出大量的热 |
C | 将CO2通入到滴有紫色石蕊溶液的水中 |
| 紫色石蕊溶液变为红色 |
D | 将打磨过的铜丝插入硝酸银溶液中 |
| 铜丝表面覆盖一层银白色物质,溶液由无色变为蓝色 |
A.AB.BC.CD.D
【题目】工业上制取烧碱的方法之一是电解食盐水法,在生成烧碱的同时还在两电极上产生两种气体(经检验均不是氧气),则该反应的化学方程式为________________________________。
某化学小组在化工商店购得某品牌的烧碱样品,准备用于化学实验。当将其配制成溶液时,小刚同学观察包装袋标签发现了问题:根据生产日期,这包烧碱存放时间较长,会不会变质呢?于是对这包烧碱进行如下探究:
(一)这包烧碱含有什么成分?
(1)打开后发现样品表面出现一层白色粉末,初步判断已经变质出现该现象的原因是_______________(用化学方程式表示);
(2)小刚同学猜想:该包烧碱的成分可能是NaOH和Na2CO3、也可能完全是Na2CO3;
(3)实验探究:
实验操作 | 现象 | 结论 |
①取少量样品于试管中.完全溶于水,加足量BaCl2溶液 | 产生白色沉淀 | 含有Na2CO3 |
②取①中上层清液,滴加____________试液 | __________________ | 还含有NaOH |
反思1:小红同学在实验完成后提出个人质疑:化学反应中的原料往往不能完全转化为产品,所以电解食盐水法制得的烧碱中往往会含有_____________杂质(填化学式)。所以需要进行再探究;
另取上述实验①中的上层清液,滴加足量稀硝酸和AgNO3溶液,产生白色沉淀,得出结论,说明小红的质疑是正确的。
反思2:小亮认为,小红的实验设计有缺陷,要想证明其结论是正确的.需要对上述实验探究作一改进后,才能得出小红质疑是正确的结论。改进的方法是____________________________。
(二)成分含量测定
a.取样品mg放入如图装置中加水完全溶解,后放在电子天平上称量为m1g;
b.打开分液漏斗活塞加入足量稀硝酸溶液,待反应停止再称量为m2g;
c.逐滴向上述反应后容器中加入M溶液至不再产生沉淀;
d.将上述混合物过滤、洗涤、烘干,称得沉淀质量为m3g。
e计算样品中Na2CO3的质量分数= ![]()
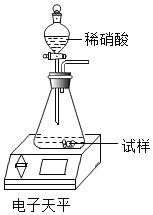
试完成下列问题:
(1)M是________________溶液(填化学式);
(2)利用沉淀物的质量(m3g)计算样品中氯化钠的质量分数,若沉淀未洗涤,则氯化钠的质量分数将_______(选填“偏大”“偏小”或“没影响”)。