题目内容
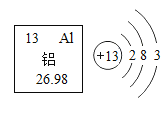
【题目】人类社会的发展离不开金属。
(1)下列物质属于合金的是_____(填标号).
a 铁矿石 b 铝 c 不锈钢 d 金刚石
(2)金属制品涂油漆可以有效防止金属锈蚀,其防锈蚀原理是__。
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是铝在高温条件下与氧化铁反应生成熔融的铁和氧化铝,该反应的化学方程式是___。
(4)向含有硝酸镁和硝酸银的废液中加入一定量的锌粉,充分反应过滤,往滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有的物质是_,滤液中一定含有的金属阳离子是__。
【答案】c 把金属和空气、水隔绝 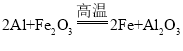 Ag Mg2+、Zn2+
Ag Mg2+、Zn2+
【解析】
(1)合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质。铁矿石没有金属特性,所以不是合金;铝是一种金属单质,属于纯净物,不是合金;不锈钢不锈钢是铁、铬、镍合金;金刚石是单质,属于纯净物,不是合金;故选c。
(2)金属暴露在空气中时容易生锈,防止金属生锈的方法通常是把金属和空气、水隔绝。
(3)根据题意可知,高温条件下,氧化铁和铝反应生成氧化铝和铁。化学方程式为: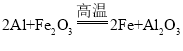 ;
;
(4)加入锌粉只能与硝酸银反应生成硝酸锌和银,不与硝酸镁反应。向滤渣中加入少量稀盐酸,无气泡产生,说明锌已完全反应。若锌粉少量,将部分银置换出来,则滤液中含有硝酸银、硝酸锌和硝酸镁,滤渣是银;若恰好完全反应,则滤液中含有硝酸锌和硝酸镁,滤渣是银;所以滤渣中一定有银,滤液中一定含有的金属阳离子是Mg2+、Zn2+。

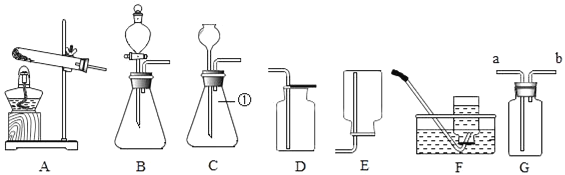
【题目】2017年合肥市中考化学实验考查D题操作中要求将稀盐酸倒入装有少量碳酸氢钠粉末的试管中,写出该反应的化学方程式______。同学们想知道反应后溶液中的溶质是什么,于是进行如下探究(假设反应中产生的气体已全部逸出):
(实验药品)石蕊溶液、酚酞溶液、铁片、铜片、氧化铁、稀盐酸、氢氧化钠溶液、氯化钠
溶液、硝酸银溶液。
(假设猜想)猜想一:氯化钠 猜想二:氯化钠、碳酸氢钠
猜想三:氯化钠、盐酸 猜想四:氯化钠、盐酸、碳酸氢钠
你认为一定错误的猜想是(简述理由):_____。
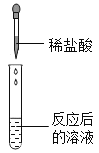
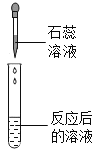
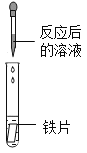
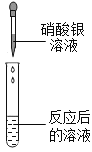
(实验探究)同学们取反应后的溶液用不同方案进行右侧表格中的相关实验。
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | 无明显现象 | 溶液变红色 | 产生气泡 | 产生白色沉淀 |
实验结论 | 猜想三正确 | |||
(得出结论)猜想三正确。写出实验方案C中发生反应的化学方程式:__。
(评价反思)老师对同学们能用多种方案进行探究并且得出正确的实验结论给予了肯定,同时指出表格中探究实验方案存在两处明显错误,请你指出这两处错误并简述理由:
错误①________;
错误②___。
(总结提高)利用上面提供的实验药品,请你再设计两个方案证明猜想三是正确的,要求写出实验操作和相应的实验现象:
方案①_____;
方案②____。
(交流讨论)如果猜想二正确,能被上述表格中实验方案_证明(填字母序号,漏填、错填不得分)。