题目内容
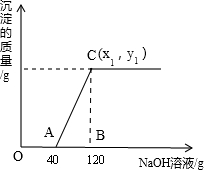
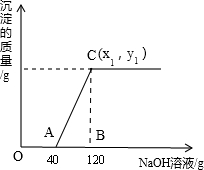
有盐酸和MgCl2的混合溶液100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的10%的NaOH溶液质量关系如图所示.若MgCl2在混合溶液中质量分数为9.5%.求:
(1)A点外溶液中的溶质化学式为 _________ .
(2)恰好沉淀完全时,所得溶液中溶质的质量分数是多少?(结果精确到0.1%) ________
(3)C点的坐标(x1,y1)为 _________ .
(2)恰好沉淀完全时,所得溶液中溶质的质量分数是多少?(结果精确到0.1%) ________
(3)C点的坐标(x1,y1)为 _________ .
(1)NaCl
(2)由图示数据可知,氢氧化钠溶液与MgCl2反应的质量为:120g﹣40g=80g,
设反应中生成的氢氧化镁沉淀的质量为x,生成氯化钠的质量为y,
2NaOH+MgCl2=2NaCl+Mg(OH)2
80 117 58
80g×10%=8g y x
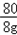 =
=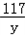 =
=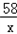 ,
,
x=5.8g; y=11.7g;
答:氢氧化镁沉淀的质量为5.8g,生成氯化钠的质量为11.7g
(3)设生成氯化钠的质量为z,
NaOH+HCl=NaCl+H2O
40 58.5
40g×10% z
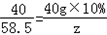
z=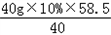 =5.85g
=5.85g
则反应至C点时溶液中溶质的质量分数为: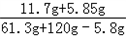 ×100%=10%.
×100%=10%.
答:反应至C点时溶液中溶质的质量分数为10%.
(2)由图示数据可知,氢氧化钠溶液与MgCl2反应的质量为:120g﹣40g=80g,
设反应中生成的氢氧化镁沉淀的质量为x,生成氯化钠的质量为y,
2NaOH+MgCl2=2NaCl+Mg(OH)2
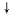
80 117 58
80g×10%=8g y x
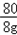 =
=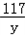 =
=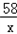 ,
,x=5.8g; y=11.7g;
答:氢氧化镁沉淀的质量为5.8g,生成氯化钠的质量为11.7g
(3)设生成氯化钠的质量为z,
NaOH+HCl=NaCl+H2O
40 58.5
40g×10% z
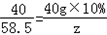
z=
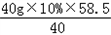 =5.85g
=5.85g则反应至C点时溶液中溶质的质量分数为:
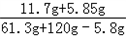 ×100%=10%.
×100%=10%.答:反应至C点时溶液中溶质的质量分数为10%.

练习册系列答案
相关题目
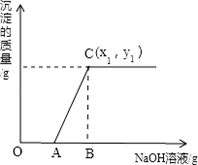
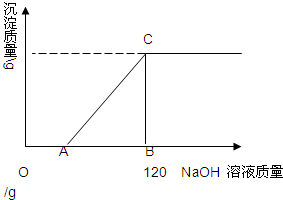 有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求:
有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求:
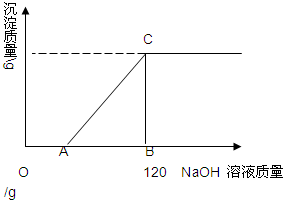 有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求:
有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求: