题目内容
【题目】根据图中实验装置,回答问题:
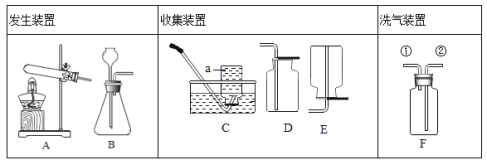
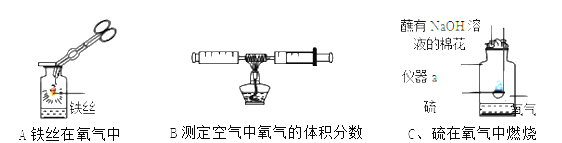
(1)仪器a的名称是_____。
(2)用A装置制取氧气的化学方程式为_____,收集装置为(填字母序号)_____。
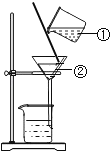
(3)实验室制取二氧化碳的化学反应方程式为_____,若用F装置收集二氧化碳,则气体应从F装置的_____(填“①”或“②”)端口通入。
【答案】集气瓶;2KMnO4![]() K2MnO4+MnO2+O2↑;C或D;CaCO3+2HCl=CaCl2+H2O+CO2↑;②;
K2MnO4+MnO2+O2↑;C或D;CaCO3+2HCl=CaCl2+H2O+CO2↑;②;
【解析】
(1)仪器a的名称是集气瓶;
(2)A装置属于固体加热型发生装置,且试管口有棉花,适宜于用高锰酸钾分解制取氧气。故用A装置制取氧气的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;由于氧气的密度比空气大且不易溶于水,故收集装置为C或D;
K2MnO4+MnO2+O2↑;由于氧气的密度比空气大且不易溶于水,故收集装置为C或D;
(3)实验室利用大理石与稀盐酸反应制取二氧化碳,反应的化学反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;由于二氧化碳的密度比空气大,若用F装置收集二氧化碳,则气体应从F装置的②端口通入。

 阅读快车系列答案
阅读快车系列答案【题目】小明、小强和小峰在学习了“质量守恒定律”后来到化学实验室亲自进行了实验探究,如图是他们分别设计的实验,请你与他们一起进行探究,并回答问题.

实验1:称量镁条,点燃,待反应结束后,再称量.
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量.
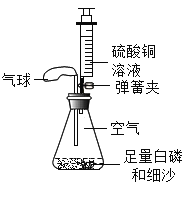
实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量.
数据见下表:(锌与盐酸反应:Zn+2HCl=ZnCl2+H2↑;氢氧化钠溶液与硫酸铜溶液反应:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4)
编号 | 实验1 | 实验2 | 实验3 |
反应前称量质量 | 9.6g | 212.6g | 118.4g |
反应后称量质量 | 16.0g | 212.4g | 118.4g |
(1)写出实验1反应的化学方程式_____.
(2)上述三个反应_____(填“符合”或“不符合”)质量守恒定律,实验_____正确反映了反应物与生成物的质量关系.
(3)由上述实验我们得到启示,探究_____的反应验证质量守恒定律,实验必须在密闭的装置中进行.
(4)由质量守恒定律可知,化学反应前后,一定不变的是_____(填序号).
①物质种类②元素种类③原子种类④分子种类⑤分子数目⑥原子数目.