题目内容
质量守恒定律的定量研究对化学发展具有重大意义.
(1)已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),m1______m2.小明在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是______.
(2)纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请你写出该反应的化学方程式______.
(1)已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),m1______m2.小明在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是______.
(2)纳米材料和纳米技术的应用涉及现代工业的各个领域.用纳米级的某种氧化物做催化剂,可以使汽车尾气中的CO和NO迅速反应转化为两种气体,其中一种是空气中含量最多的气体.请你写出该反应的化学方程式______.
(1)根据质量守恒定律,生成氧化镁的质量=参加反应的镁的质量+氧气的质量,所以m1小于m2;镁带燃烧时放出耀眼的白光,放出大量的热,放出大量的白烟,仔细观察会发现:白烟有很大一部分向上,生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中导致m1>m2.
(2)依据其中一种是空气中含量最多的气体确定一种物质是氮气,依据化学反应前后元素的种类不变确定一种生成物是二氧化碳,从而得到化学方程式是:2CO+2NO
N2+2CO2
故答案为:(1)<;生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中(2)2CO+2NO
N2+2CO2
(2)依据其中一种是空气中含量最多的气体确定一种物质是氮气,依据化学反应前后元素的种类不变确定一种生成物是二氧化碳,从而得到化学方程式是:2CO+2NO
| ||
故答案为:(1)<;生成物氧化镁部分以白烟的形式逸散(或扩散)到空气中(2)2CO+2NO
| ||

练习册系列答案
相关题目
 ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: 由“
由“ ”聚集成的物质
”聚集成的物质 质量守恒定律的定量研究对化学科学发展具有重大意义.
质量守恒定律的定量研究对化学科学发展具有重大意义. ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: ”聚集成的物质
”聚集成的物质 ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: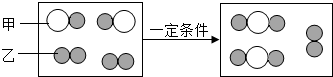
 ”聚集成的物质
”聚集成的物质