题目内容
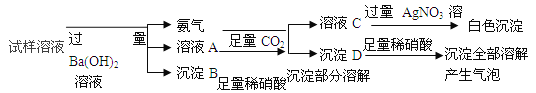
【题目】蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如图所示:
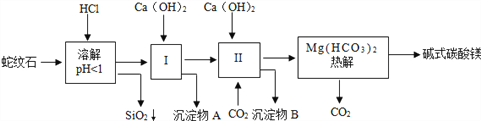
查阅资料:A.几种物质沉淀和溶解时的 pH 如下表
氢氧化物 | 溶液 pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
B.难溶性碱加热会生成两种氧化物,各元素化合价都不变。
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是________(用化学方程式表示)。
(2)进行操作Ⅰ时,需控制溶液pH=6~7,Ca(OH)2不能过量。若Ca(OH)2过量, 可能导致_______溶解、________沉淀。
(3)从沉淀混合物 A 中提取红色氧化物作颜料,先向沉淀物 A 中加入________(填物质的化学式),然后_________、________、灼烧(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______。
探究二:确定产品碱式碳酸镁(mMgCO3·nMg(OH)2·xH2O)的组成,组装如图 1 仪器:
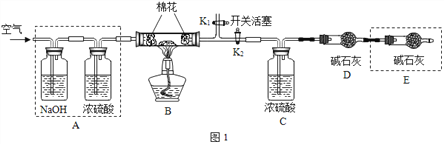
实验测得:硬质玻璃管中剩余的固体质量为 2.0g,C 处浓H2SO4增重 0.9g,D 处碱石灰增 重 1.76g。
(1)在装好试剂后,加热前应进行的操作是_______;
(2)A 框中装置的作用是________;
(3)通过计算写出碱式碳酸镁的化学式__________。(请写出计算过程)
【交流与反思】
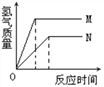
(1)若将 E 框中的装置去掉,对实验结果的影响是 m
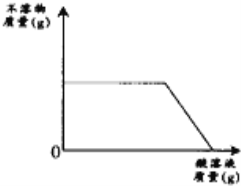
(2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物。为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图 2 坐标系,试回答。
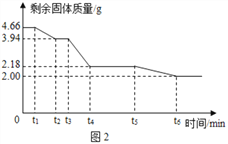
①t4~t5时间段固体的化学式为__________;
②t5~t6时间段发生反应的方程式为___________。
【答案】 Ca(OH)2 + 2HCl = CaCl2 + 2H2O Al(OH)3 Mg(OH)2 NaOH 过滤 洗涤 CO2 检查装置气密性 除去空气中的CO2和H2O 4MgCO3·Mg(OH)2·4H2O 偏大 偏大 MgO 、Mg(OH)2 Mg(OH)2 ![]() MgO + H2O
MgO + H2O
【解析】探究一:(1)盐酸和氢氧化钙会发生中和反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
(2)由(1)知,此时溶液中除了Mg2+外,还含有Fe3+、Al3+杂质,需除去Fe3+、Al3+但不能损失Mg2+,因Fe3++3H2O![]() Fe(OH)3+3H+和Al3++3H2O
Fe(OH)3+3H+和Al3++3H2O![]() Al(OH)3+3H+,利用平衡移动的原理,消耗H+使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,加Ca(OH)2需将溶液的pH控制在7~8,若pH过高,会导致生成的Al(OH)3发生反应Al(OH)3+OH-=AlO2-+2H2O溶解,Mg(OH)2在pH为9.4时开始沉淀,所以碱性增强Mg(OH)2会沉淀,同时Mg2+也因转化为沉淀而损失,所以可能导致Al(OH)3溶解,Mg(OH)2沉淀;
Al(OH)3+3H+,利用平衡移动的原理,消耗H+使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,加Ca(OH)2需将溶液的pH控制在7~8,若pH过高,会导致生成的Al(OH)3发生反应Al(OH)3+OH-=AlO2-+2H2O溶解,Mg(OH)2在pH为9.4时开始沉淀,所以碱性增强Mg(OH)2会沉淀,同时Mg2+也因转化为沉淀而损失,所以可能导致Al(OH)3溶解,Mg(OH)2沉淀;
(3)从实验步骤图知:沉淀混合物为Fe(OH)3和Al(OH)3,红色氧化物是沉淀物Fe(OH)3分解后得到的Fe2O3,所以得先加碱把Al(OH)3除掉,反应为:Al(OH)3+NaOH=NaAlO2+2H2O,然后过滤、洗涤、灼烧即可;
探究二:(1)仪器连接后,需要进行的操作是:检验装置气密性;
(2)浓硫酸有吸水性,氢氧化钠溶液可以吸收空气中的二氧化碳,避免对后面检验二氧化碳、水造成干扰,所以A框中装置的作用是:除去空气中的二氧化碳和水;
(3)硬质玻璃管中剩余的固体质量为2.0g,C处浓H2SO4增重0.9g,所以m(H2O)=0.9g,D处碱石灰增重1.76g,所以m(CO2)=1.76g,
mMgCO3nMg(OH)2xH2O![]() (m+n)MgO+mCO2↑+(n+x)H2O↑,
(m+n)MgO+mCO2↑+(n+x)H2O↑,
80(m+n)44m 18(n+x)
2g 1.76g 0.9g
![]()
解之得:m=4,n=1,x=4,
所以碱式碳酸镁的化学式为:4MgCO3Mg(OH)24H2O;
【交流与反思】(1)将E框中的装置去掉,空气中的二氧化碳和水蒸气会增加碱石灰和浓硫酸的质量,所以对实验结果的影响是m值偏大,x值偏大;
(6)通碱式碳酸镁在分解时先失去结晶水,然后碳酸镁开始分解,最后氢氧化镁开始分解,所以t4~t5时间段固体为:Mg(OH)2和MgO;
t5~t6时间段发生的反应是氢氧化镁在加热的条件下生成氧化镁和水,化学方程式为:Mg(OH)2 ![]() MgO + H2O。
MgO + H2O。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案