题目内容
【题目】小涛同学在实验室里用过氧化氢溶液制取氧气,他取了68.0g过氧化氢溶液,加入1.0g二氧化锰,待完全反应后,称得剩余固体与液体的混合物的总质量为65.8g(不考虑反应过程中水分的蒸发),请回答下列问题:(本题计算结果均精确至0.1g)
(1)反应结束后,过滤得到滤渣的质量为_____g,二氧化锰是该反应的_____。
(2)该同学制得的氧气质量为_____g。
(3)原过氧化氢溶液中氢元素的质量为_____g。
(4)根据化学方程式计算,过氧化氢溶液中过氧化氢的质量_____。
【答案】1 催化剂; 3.2g; 7.2g; 6.8g。
【解析】
(1)二氧化锰是过氧化氢分解的催化剂,在化学反应前后,质量保持不变,所以反应结束后,过滤得到滤渣的质量为1g;
(2)根据质量守恒定律可得,生成的氧气的质量为68.0g+1g﹣65.8g=3.2g;
(3)原过氧化氢溶液中氢元素的质量为:(65.8g﹣1g)×![]() ×100%=7.2g;
×100%=7.2g;
(4)设过氧化氢的质量为x
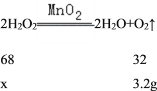
![]()
x=6.8g

练习册系列答案
相关题目