题目内容
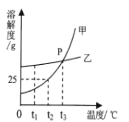
【题目】请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
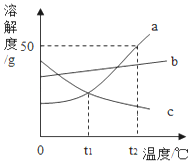
(1)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后, 所得溶液的质量为_______g。
(2)若b物质中混有少量a物质,最好采用____________的方法提纯。
(3)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是________________。
(4)下列说法正确的是_______________。(填序号)
A 将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B 将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
C 配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高。
【答案】75 蒸发结晶 cba BC
【解析】
a的溶解度随着温度的升高逐渐增大,b的溶解度随温度的增大增长趋势较慢,c的溶解度随温度的升高而减少,交点表示两者的溶解度相同。
(1)在t2℃时,a物质的溶解度为50g,表示在t2℃时,100g水中可以溶解50g的a物质,向盛有50ga物质的烧杯中加入50g水,可以溶解的a的质量为25g,充分溶解后, 所得溶液的质量为50g+25g=75g。
(2)b物质的溶解度随温度变化较小,提纯b用蒸发结晶的方法,若b物质中混有少量a物质,最好采用蒸发结晶的方法提纯。
(3)t2℃时,a、b、c三种物质的饱和溶液各100g,a中含有的溶质质量为50g,b中含有的溶质质量小于50g,c中含有的溶质质量比b还少,溶剂质量=溶液质量溶质质量,所以含溶剂的质量由大到小的顺序是c、b、a。
(4)
A、将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数不一定减小,如升高温度使a的饱和溶液变为不饱和溶液,溶质质量发生不变,故A不正确;
B、将t1℃时c物质的饱和溶液升温到t2℃,c的溶解度减小,溶液中有晶体析出,溶液的质量减小,故B正确;
C、配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,读数偏大,量取水的体积偏小 ,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高,故C正确。故选BC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
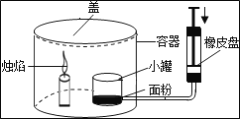
小学生10分钟应用题系列答案【题目】在介绍氢气的制法时,老师告诉同学们,铝丝与一种可以用铁制容器盛装的溶液反应,也会生成氢气。
(提出问题)与铝丝反应的是什么溶液?
(交流讨论)分析后,大家一致认为该溶液不是稀盐酸或稀硫酸,原因是_____。
同学们决定进一步探究。老师为同学们提供了该溶液。
(查阅资料)含有不同金属离子的溶液在灼烧时会产生不同颜色的火焰
钠 | 钙 | 钾 |
黄色 | 砖红色 | 紫色(透过蓝色钴玻璃) |
(实验探究)
①小强取该溶液于试管中,向其中滴加紫色石蕊溶液,发现紫色石蕊溶液变蓝。
②小明用铂丝蘸取该溶液在酒精灯火焰上灼烧,观察到火焰呈黄色。
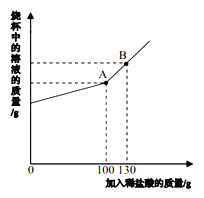
③有同学提出应向该溶液中滴加稀盐酸,小美取该溶液于试管中,向其中加入足量的稀盐酸后,没有看到明显现象,这样做是为了排除_____(填离子符号)的干扰。
(实验结论)该溶液为_____溶液。
(交流反思)
①老师告诉同学们,铝与该溶液反应除了生成氢气外,还生成了一种含有A1O2﹣的盐,请写出该反应的化学方程式_____。
②金属铝的化学性质较活泼,而生活中使用的铝制品却耐腐蚀,原因是_____。
【题目】某化学兴趣小组的同学在实验室发现一瓶敞口放置的过氧化钠(Na2O2)固体,他们对该固体是否变质产生了兴趣,对固体成分进行了实验探究。
(查阅资料)
①在标准状况下,氧气的密度是1.429g/L.在室温下,1L水中能溶解约30mL的氧气。
②过氧化钠能与二氧化碳反应:2Na2O2+2CO2═2Na2CO3+O2↑
③过氧化钠能与水反应:2Na2O2+2H2O═4NaOH+O2↑
④BaCl2溶液呈中性。
(成分猜想)固体中可能有Na2O2、NaOH和Na2CO3中的一种或几种。
(实验验证)
实验步骤 | 实验现象 | 结论或化学方程式 |
(1)取少量样品于试管中,加水溶解,并立即将带火星的木条伸入试管中。 | 有气泡产生,_______ | 证明固体中含有Na2O2 |
取步骤(1)所得溶液于试管中,滴加过量的BaCl2溶液 | 有白色沉淀生成 | 证明固体中含有Na2CO3,化学方程式为_______ |
取步骤(2)中的上层清液于试管中,滴入1~2滴酚酞试液 | 溶液变红 | 证明固体中含有NaOH. |
(分析交流)经过讨论分析,同学们认为步骤(3)中的结论不合理,不能证明固体中含有NaOH,理由是_______。
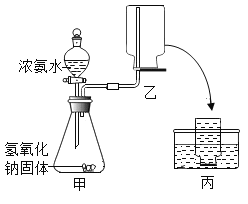
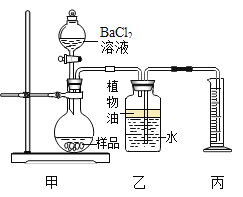
(继续探究)为确定固体中是否含有NaOH,取一定质量的样品,利用如图装置进行实验验证。(BaCl2溶液的体积和温度变化对气体体积的影响忽略不计)
(1)装置乙中植物油的作用是_______。
(2)待反应完全后,根据收集所得气体的体积,进行相关计算,得出样品中_______的质量。
(3)再将烧瓶中的沉淀进行过滤、洗涤、烘干、称量,进行相关计算,得出样品中_______的质量。
(实验结论)经过实验数据分析,得出固体中不但含有Na2O2和Na2CO3,还含有NaOH.证明含有NaOH的依据是_______。