��Ŀ����
����Ŀ��ͬѧ���Ѿ�ѧϰ�������Ͷ�����̼��ʵ�����Ʒ�����������ܽ��������

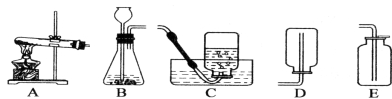
��������ʶ��װ��A�����������ƣ�a ��1�� ��b ��2�� ��װ��C�����ƣ� ��3��
����Ӧԭ������˫��ˮ�Ͷ������̻����ȡ�����Ļ�ѧ����ʽΪ ��4�� ��
�ô���ʯ��ϡ������ȡ������̼�Ļ�ѧ����ʽΪ ��5�� ��
����ȡװ����������������������ȡ��������ѡ�õķ���װ���� ��6�� �����ռ��ϴ������������ѡ�� ��7�� װ�ã������������� ��8�� ��
ʵ������ȡ������̼���壬��ѡ�õ�װ������� ��9�� �� ��10�� ��
���������̼�Ƿ������ķ����� ��11�� ������ʵ�������������ۣ���
�Ƚ�B��Cװ�ã�Cװ������ȡ����ʱ�����Ե��ŵ��� ��12�� ��
�����ݷ�����ʵ��С��������غͶ������̵Ļ������ȡ��������Ӧ�����������������仯��ͼ��ʾ����ȫ��Ӧ�������ռ���0.3 mol������

������ݻ�ѧ����ʽ��ʽ����ԭ������к�����ص���������13��
��ͼ��P�㴦�Թ��ڵĹ��������� ��14��
��������1���Թ� ��2������̨ ��3�����շ����� ��4��2H2O2 ![]() 2H2O +O2��
2H2O +O2��
��5��CaCO3 + 2HCl==CaCl2 + CO2�� + H2O��6��A ��7��F ��8������ƿ���������ݳ�������ƿ��ˮ�ž��� ��9��BE ��10��CE ��11����ȼ����ľ�����ڼ���ƿ����Ϩ������ʾ�����ˣ�12�����Կ��Ʒ�Ӧ��ʼ�������13��24.5 g��14���������̡��Ȼ��ء������
��������
���������������������������ȡ������Ҫ��������ѡ��Aװ�ã�������̼����ȡ��Ҫ��������ѡ��Bװ�ã����������̼�Ƿ������ķ�������ȼ�ŵ�ľ������ƿ�ڴ����������Ϩ��˵�����ˣ�Cװ������ȡ����ʱ�����Ե��ŵ�����ʱ���أ����ڿ��Ʒ�Ӧ��
�裺ԭ������������Ϊx mol
2KClO3![]() 2KCl+3O2��
2KCl+3O2��
2 3
x mol 0.3 mol
![]() ��1�֣�
��1�֣�
x = 0.2 mol��1�֣�
���������=0.2 mol��122.5g/mol=24.5 g

����Ŀ����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ������ͼʾ�ش����⣺
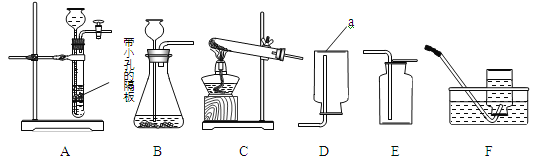
�������a������ ��6�� ��
��ʵ�����ô���ʯ��ϡ������ȡ������̼��������Ӧ�Ļ�ѧ����ʽΪ ��7�� ��
ͨ������̼��Ʒ�ĩ��ϡ���ᷴӦ��ȡCO2��ԭ���� ��8�� ����Ҫ��ȡ���ռ�һƿCO2������ʹ��Ӧ�����ͣ��ѡ�õ�װ������� ��9�� ������ĸ����֤��������̼���ռ����ķ����� ��10�� ��
��ʵ������˫��ˮ�Ͷ������̷�ĩ��ȡ����ʱ���ڶ������̵Ĵ������£���������Ѹ�ٷֽ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ ��11�� ����Щ���ػ�Ӱ���Ź�������ֽ�����ʣ���С��̽�����������������Թ�������ֽ��������Ӱ�죬��С������˸������̽�����¶��Ƿ�Ӱ���Ź�������ֽ�������أ�
ʵ �� �� �� | �� �� | �� �� |
ȡһ֧�Թܣ�����5mL5%�Ĺ���������Һ��Ȼ����Թܷ���ʢ����ˮ���ձ��У� | ���������� ����ð�� | ��13�� |
��ȡһ֧�Թܣ����� ��12�� �� Ȼ����Թܷ���ʢ����ˮ���ձ��С� | Ѹ���д��� ����ð�� |
����С����װ��C��ȡ�������Թ��й�������������ʱ��仯�����ݼ��±�����Ӧ������ʣ�����������ˮ����ܽ���ˣ����ն������̹��壬���õ��Ȼ�����Һ100g��
����ʱ��/min | 0 | t1 | t2 | t3 |
��������/g | 28.0 | 23.2 | 18.4 | 18.4 |
��I����װװ��Cʱ��������������Ʒ����װ˳���� ��14�� ������ţ���
a���Թ� b������̨ c���ƾ��� d��ľ��
��II�����Ƶ����������ʵ���Ϊ ��15�� mol��
��III�������Ȼ�����Һ�������������������ݻ�ѧ����ʽ��ʽ���㣩 ��16�� ��
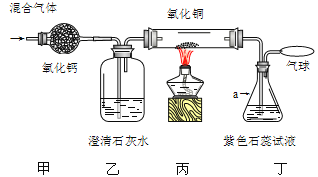
����Ŀ��Ϊ��֤ij����������Ƿ���һ����̼��������̼ ��ˮ������ͬѧ���������ʵ��װ�ã�װ�����������ã����������������ͨ�롣ʵ�������¼���¡���ҩƷ��������ÿ����Ӧ��ȫ���г�����ʡ�ԣ�
װ�� | ���� |
�� | ���� |
�� | ���������� |
�� | ��ĩ�� ��� |
�� | ��Һ���ϱ�죬������ |
������a������ ��21�� ��
���з�ĩ�� ��22�� ��죬�����Ļ�ѧ��Ӧ����ʽΪ ��23�� ����������ͭ�� ��24�� ����
���������������������������һ������ˮ������һ����̼�����ܺ���������̼��д�����ܺ��ж�����̼������ ��25�� ��
�����ڲ��ı�װ�õ�ǰ���£�ֻ�轫װ�� ��26�� ��ҩƷ���� ��27�� �������ж϶�����̼�Ƿ���ڡ�