题目内容
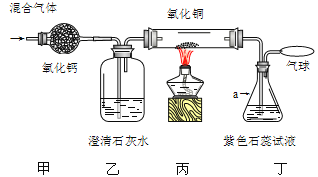
【题目】为验证某混合气体中是否含有一氧化碳、二氧化碳 和水蒸气,同学设计了如下实验装置(装置气密性良好),将混合气体依次通入。实验现象记录如下。(药品均足量且每步反应完全、夹持仪器省略)
装置 | 现象 |
甲 | 增重 |
乙 | 无明显现象 |
丙 | 粉末由 变红 |
丁 | 试液由紫变红,气球变大 |
Ⅰ.仪器a的名称 (21) 。
Ⅱ.丙中粉末由 (22) 变红,发生的化学反应方程式为 (23) ,其中氧化铜作 (24) 剂。
Ⅲ.根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳。写出可能含有二氧化碳的理由 (25) 。
Ⅳ.在不改变装置的前提下,只需将装置 (26) 中药品换成 (27) ,即可判断二氧化碳是否存在。
【答案】(21)锥形瓶(22)黑(23)CuO+CO![]() Cu+CO2;(24)氧化;(25)甲中氧化钙吸收水蒸气生成氢氧化钙,如含有CO2会与氢氧化钙反应,导致乙中无明显现象;(26)甲(27)CuSO4
Cu+CO2;(24)氧化;(25)甲中氧化钙吸收水蒸气生成氢氧化钙,如含有CO2会与氢氧化钙反应,导致乙中无明显现象;(26)甲(27)CuSO4
【解析】
试题分析:有题中图可知Ⅰ.仪器a的名称为锥形瓶;Ⅱ.丙中粉末由黑色变红,发生的化学反应方程式为CuO+CO![]() Cu+CO2;,其中氧化铜提供氧元素,作氧化剂;Ⅲ.根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳 。可能含有二氧化碳的理由甲中氧化钙吸收水蒸气生成氢氧化钙,如含有CO2会与氢氧化钙反应,导致乙中无明显现象; Ⅳ.在不改变装置的前提下,只需将装置 甲 中药品换成无水硫酸铜,即可判断二氧化碳是否存在。
Cu+CO2;,其中氧化铜提供氧元素,作氧化剂;Ⅲ.根据上述现象,分析混合气体中一定含有水蒸气、一氧化碳,可能含有二氧化碳 。可能含有二氧化碳的理由甲中氧化钙吸收水蒸气生成氢氧化钙,如含有CO2会与氢氧化钙反应,导致乙中无明显现象; Ⅳ.在不改变装置的前提下,只需将装置 甲 中药品换成无水硫酸铜,即可判断二氧化碳是否存在。

练习册系列答案
相关题目