题目内容
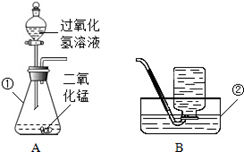
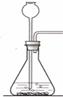
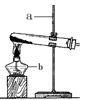
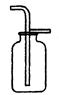
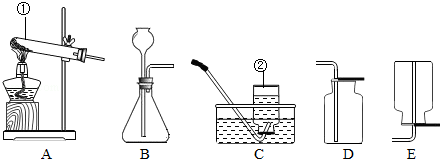
(6分)如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题: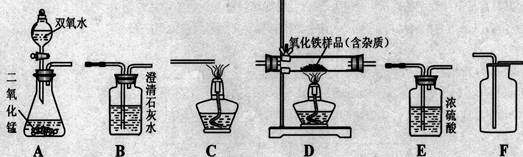
(1) 欲在实验室中制备并收集干燥的氧气。
① 所选仪器的连接顺序为 (填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为 。
(2) 欲用足量纯净的一氧化碳气体测定某不纯氧化铁样品的纯度 (杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:纯净的一氧化碳气体 →D→B→C。
①仪器C的作用是 。
②仪器D中发生的化学反应方程式为
③反应完全后,计算氧化铁样品的纯度时,小强同学认为“仪器D中减少的质量等于仪器B中增加的质量”。小丽同学通过称量发现二者质量并不相等。请你分析写出仪器D中减少的是 ________的质量,而仪器B中增加的是 _________的质量。
(1)①AEF ②2H 2O 2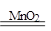 2H 2O+O 2↑
2H 2O+O 2↑
(2) ①将多余的CO燃烧掉,防止污染空气或使人中毒。(其他合理答案均可)
②3CO+Fe2O3 3CO2+2Fe
3CO2+2Fe
③氧化铁(或Fe2O3)中的氧(或O)元素 ; 反应生成的二氧化碳(或CO2)
解析试题分析:利用浓硫酸的吸水性,所以常用浓硫酸来干燥气体,所以在实验室中制备并收集干燥的氧气,应选择的装置为AEF,过氧化氢制氧气的反应原理为2H 2O 2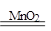 2H 2O+O 2↑;CO有毒,所以在实验中需将尾气进行处理,常用燃烧法将有毒的一氧化碳转化为无毒的二氧化碳,防止污染空气,炼铁的原理为:3CO+Fe2O3
2H 2O+O 2↑;CO有毒,所以在实验中需将尾气进行处理,常用燃烧法将有毒的一氧化碳转化为无毒的二氧化碳,防止污染空气,炼铁的原理为:3CO+Fe2O3 3CO2+2Fe;仪器D中减少的质量低于仪器B中增加的质量,是因为D中减少的是氧化铁(或Fe2O3)中的氧(或O)元素,而仪器B中增加的是二氧化碳得质量。
3CO2+2Fe;仪器D中减少的质量低于仪器B中增加的质量,是因为D中减少的是氧化铁(或Fe2O3)中的氧(或O)元素,而仪器B中增加的是二氧化碳得质量。
考点:气体的制取、除杂与收集

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案除去下列物质中混有的少量杂质(括号内为杂质)的方法中,正确的是
| A.CO2(HCl):混合气体通过澄清石灰水后干燥 |
| B.CuO(炭粉):混合物中滴加稀盐酸后过滤、烘干 |
| C.NaCl溶液(CaCl2):混合物中滴加适量碳酸钠溶液后过滤 |
| D.NaOH溶液(Na2CO3):混合物中滴加适量氯化钙溶液后过滤 |
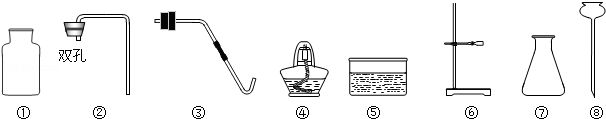

 2H2O + O2↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是 。
2H2O + O2↑,在实验室利用此反应制取氧气时,应选用的气体发生装置是 。