题目内容
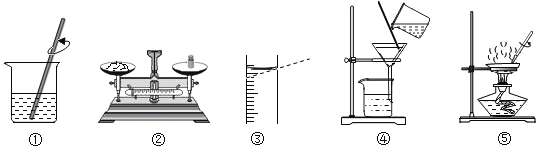
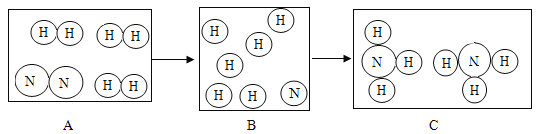
【题目】下列图象与对应实验完全吻合的是
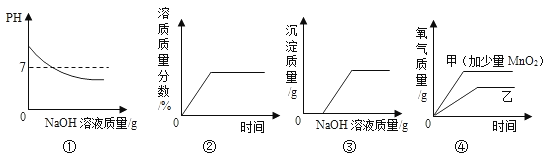
A.①往一定量的盐酸中滴加NaOH溶液至过量
B.②将一定量的不饱和KNO3溶液恒温蒸发水
C.③向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
D.④用两份等质量等溶质质量分数的过氧化氢溶液制取氧气(甲加少量MnO2)
【答案】C
【解析】
A、盐酸呈酸性,其pH小于7,而图象开始pH大于7,故A错误;
B、不饱和KNO3溶液恒温蒸发水,其溶质的质量分数逐渐增大,当饱和时不再改变,开始时其溶质质量分数不是0,故B错误;
C、硫酸铜与氢氧化钠反应生成的氢氧化铜沉淀能与硫酸反应生成硫酸铜,故在硫酸铜和稀硫酸的混合液中硫酸首先与氢氧化钠反应,硫酸铜后与氢氧化钠反应,也就是刚开始不能出现硫酸铜沉淀,故C正确;
D、两份等质量等溶质质量分数的过氧化氢溶液反应生成氧气的质量相同,故D错误.
故选C.

【题目】某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小丽要测定某地采集到的雨水是否为酸雨,已知pH小于5.6的降水称为酸雨,下列提供的试剂(试纸)中宜取用_______
A 蓝色石蕊试纸 B 紫色石蕊溶液 C 无色酚酞试剂 D pH试纸
(2)小刚探究氢氧化钙的化学性质时分别用澄清石灰水与以下四种物质反应:

I.写出小刚进行的四个实验中无明显现象产生的反应的化学方程式____。
II.若采用另一种盐的溶液取代Na2CO3溶液与澄清石灰水反应,小刚应选择的物质是__。
A BaCl2 B NaCl C FeCl3 D Ba(NO3)2
(3)小雨对碳酸钙高温加热一段时间,得到一些剩余固体。她对这些剩余固体的成分进行了探究。
(提出问题)剩余固体成分是什么?
(猜想与假设)剩余固体成分为:
A 全部是碳酸钙 B 既有碳酸钙,也有氧化钙 C 全部是氧化钙
(设计并完成实验)
实验操作 | 实验现象 | 实验结论 |
a. 取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有__ |
b.再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有___ |
(实验结论)该化学兴趣小组同学得出的结论:
剩余固体成分与(猜想与假设)中的______ (填“A”“B”或“C”)符合。
(交流与反思)实验操作b产生的气体是_______,如何检验是该气体________;剩余固体的成分若与C相符,则两步操作的实验现象_____(填“a”或“b”或“ab”)不同。