题目内容
【题目】如图是镁元素和硫元素在元素周期表中的信息和四种粒子的结构示意图。请回答下列问题: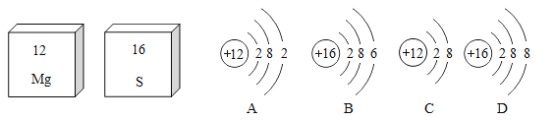
(1)镁原子的核电荷数是____________;镁元素与硫元素的最本质区别是________。
(2)在镁和硫生成硫化镁的反应中,得到电子的是____________原子;镁离子的结构示意图是(填字母)____________.
(3)C和D构成化合物的化学式为____________.
【答案】12 质子数不同 硫 C MgS
【解析】
(1)由元素周期表方格的信息可知镁原子序数为12,根据原子序数=核电荷数=质子数可知镁原子原子的核电荷数也为12,故填12;不同元素最本质的区别是核电荷数(质子数)不同;故填核电荷数不同;
(2)根据硫元素的原子结构示意图B可知,硫原子的最外层电子数是6,在反应中易得到电子形成带两个单位负电荷的硫离子,即结构示意图为D,故填硫;在微粒结构示意图中若质子数>核外电子数,则为阳离子,再根据镁元素的质子数为12可判断C图为镁离子结构示意图,故填C;
(3)由上分析可知C是镁离子,质子数比核外电子数多2,可知镁离子带有2个单位的正电荷,D是硫离子带有2个单位的负电荷,根据化合物中各元素化合价代数和为零可知二者构成的化合物的化学式为MgS,故填MgS。

练习册系列答案
相关题目