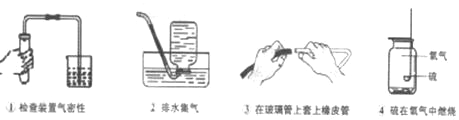
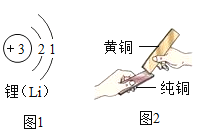
��Ŀ����
����Ŀ��MnO2����������صķֽ������ã��Թ�������ķֽ�Ҳ�����á�д�������������������̷�Ӧ�����ֱ���ʽ��ѧ����ʽ��_____��
ijͬѧ�룺CuO�ܷ�������MnO2�Ĵ��������أ����ǽ���������̽����
�����룩I��CuO���Ǵ�����Ҳ�����뷴Ӧ����Ӧǰ�������ͻ�ѧ���ʲ��䣻
II��CO���뷴Ӧ����O2����Ӧǰ�������ͻ�ѧ�ʷ����˸ı䣻
��CuO�Ƿ�Ӧ�Ĵ�������Ӧǰ��_____��
��ʵ�飩����ƽ����0.2g CuO��ȡ5mL5%�Ĺ���������Һ���Թ��У���������ʵ�飺

��1��������
��������� | ������ | ��������� | ���� |
_____ | _____ | _____ | ��������� ���������� |
��2������ٵ�Ŀ����_____��
��3�����������ܱ�CuO���ֽ����O2�Ļ�ѧ����ʽΪ_____��
���𰸡������![]() �Ȼ���+������2KClO3
�Ȼ���+������2KClO3![]() 2KCl+3O2�� �����ͻ�ѧ���ʲ��� ��Һ�������ݷų��������ǵ�ľ����ȼ CuO������Ϊ0.2g ��Һ�������ݷų��������ǵ�ľ����ȼ �벽��۶Աȣ��������CuOǰ��˫��ˮ�ķֽ��ٶ����ޱ仯 2H2O2
2KCl+3O2�� �����ͻ�ѧ���ʲ��� ��Һ�������ݷų��������ǵ�ľ����ȼ CuO������Ϊ0.2g ��Һ�������ݷų��������ǵ�ľ����ȼ �벽��۶Աȣ��������CuOǰ��˫��ˮ�ķֽ��ٶ����ޱ仯 2H2O2![]() 2H2O+O2��
2H2O+O2��
��������
��������غͶ������̻����ķ�Ӧ���ֱ���ʽ�������![]() �Ȼ���+��������ѧ����ʽΪ��2KClO3
�Ȼ���+��������ѧ����ʽΪ��2KClO3![]() 2KCl+3O2����
2KCl+3O2����
�����������ص�����һ�䣬��������������Ӧ���ʱ䣬�����ͻ�ѧ���ʲ��䣻
��1������ͭ�Թ�������ķֽ��д����ã��ܼӿ���ֽ������������������ʣ���������������ð���������ǵ�ľ����ȼ���������ص�����һ�䣬������������Ӧǰ�����������䣬��������ͭ��������Ϊ0.2g���������ص�����һ�䣬�������������з�Ӧ���ʸı䣬�����Ǽӿ죬��ѧ���ʲ��䣬�Կ�����������������������Һ�������ݷų��������ǵ�ľ����ȼ��
��2��Ϊ�˿�����ͭ�Ƿ��ܸı䷴Ӧ�����ʣ�Ҫͨ����������ͭ�벻������ͭ��������жԱȣ����ܵó���ѧ�����Ľ��ۣ�
��3�����������ܱ�����ͭ���ֽ�ų�O2�Ļ�ѧ����ʽΪ��2H2O2![]() 2H2O+O2����
2H2O+O2����

 ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�����Ŀ�����ݵ���ʯ��ʯ��Դ�ḻ��ij��ѧ��ȤС���ȡ4.0gʯ��ʯ��Ʒ����40gϡ�����4�μ�����Ʒ��(�������ʲ���ӦҲ���ܽ�)����ʵ���������£�
ϡ��������� | ʣ���������� |
��һ�μ���10g | 3.0g |
�ڶ��μ���10g | 2.0g |
�������10g | 1.0g |
���Ĵμ���10g | 0.6g |
����㣺
(1)4.0gʯ��ʯ��Ʒ��̼��Ƶ�������____g��
(2)10gϡ��������_____g̼���������ȫ��Ӧ��
(3)��ϡ�����������������Ϊ_________(д��������̣������ȷ��0.1%)
����Ŀ����Һ�����ǵ���������������ء�
��1�������KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ��ش����⡣
�¶�/�� | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
�ܽ��/g | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 |
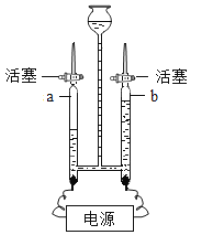
90��ʱ����һ��������KNO3��Һ��ͼ1ʾ���в�����

90��ʱ��KNO3��Һ��______����������������������������Һ��ͼ��n����ֵΪ______��
��2���������ͼ2�мס��ҡ������ֹ�����ܽ�����ش����⡣
T3��ʱ���ڸ����мס��ҡ���30�˹���������ձ��У��ֱ���50��ˮ����ֽ�����γɱ�����Һ����______���¶Ƚ�����T2��ʱ����������Һ�����ʵ����������ɴ�С��˳��Ϊ______��
T3��ʱ100��ˮ�м���95�˼Ĺ��壬����ȫ���ܽ⣬һ��ʱ������в��ּĹ�����������ȫ���ܽ�����ԭ������ǣ�______��
����Ŀ��ij����С���������ʵ��̽����
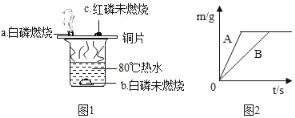
��1����֤���ʵ�ȼ������
����ͼ1����ʵ�飬ʵ��������ͼ��ʾ��
��80����ˮ��������_____��_____��
���Ƚ�����a��c���ó�ȼ�յ�������_____��
��2������һ��������п��Ͷ�뺬��Cu��NO3��2��Fe��NO3��2�Ļ����Һ�У���ַ�Ӧ����ˣ�����Һ��ֻ��һ�����ʣ���������һ������_____�����ѧ���
����������ȡ���������������ͬ��ϡ�����У��ֱ�����������п�ۺ����ۣ���������������m���淴Ӧʱ�䣨t���ı仯������ͼ2��ʾ�����б�������ȷ����_____������ţ���
��A��ʾп��ϡ����ķ�Ӧ���� ����Ӧ�������������ֽ������������
����Ӧ���������ֽ���һ������ʣ�� ����Ӧ������ϡ���ᶼû��ʣ��
����Ӧ���������ɵ�����������ȡ�
��3����AgNO3��Mg��NO3��2�Ļ����Һ�м���һ���������ۣ���ַ�Ӧ����ˣ��������е���ϡ���ᣬ����ɫ��������������ж���������Һ�ijɷ��ж��У���ȷ����_____������ĸ����
A����Һ������ֻ��Fe��NO3��2 B����Һ�Щ�������Fe��NO3��2��Mg��NO3��2
C�� ������ֻ���� D��������һ������������
��4����ѧ�ҷ���һ���½����������±���Ϣ�Ʋ�ý������ʺϵ���;��_____��
�۵� | �ܶ� | ǿ�� | ������ | ������ | ����ʴ�� |
2500�� | 3g/cm3 | ������� | ���� | ���� | ���� |
A�����ӽ��� B������ͨѶ�豸 C��������������� D�����캽��ɻ�
��5���ⶨˮ���⡢��Ԫ�ص������ȡ�����ͼ3����ʵ�飬��Ӧ���ü��в����ܣ���ҩƷ����������ag������U�ιܣ���ҩƷ����������bg��
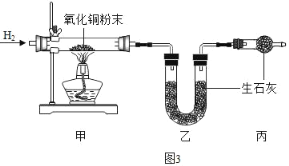
��ˮ���⡢��Ԫ�ص���������_____���ú� a��b��ʽ�ӱ�ʾ����
�����������У��Բⶨ���û��Ӱ�����_____������ţ���
A��CuO��ĩ������ B��CuOû����ȫת��ΪCu C��û�б�װ��