题目内容
(2010?石狮市)下图是元素周期表的一部分.已知从左到右元素的性质呈现以下特点:金属性逐渐减弱,非金属性逐渐增强;金属对应的碱碱性逐渐减弱,非金属对应的酸酸性逐渐增强.回答以下问题:
①.推测X是
②.原子序数为11、13的两元素的金属活动性强弱为(用元素符号表示):
③.原子序数为16号的元素Y对应的酸化学式为H2YO4,其中Y的化合价为
④.原子序数为15的元素形成酸的化学式为H3PO4原子序数为16的元素形成酸的化学式为H2SO4,其中酸性较弱的是(用化学式表示)
⑤.铝在实际生活中既能跟酸反应,也能与部分碱反应,如果将铝放入热的氢氧化钠水溶液中,将生成偏铝酸钠(NaAlO2)和氢气,试写出此反应的化学方程式
| 11 Na 钠 | 12 X 镁 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 Y 硫 硫 | 17 Cl 氯 |
金属
金属
元素,Y是非金属
非金属
元素.(选填“金属或非金属”)②.原子序数为11、13的两元素的金属活动性强弱为(用元素符号表示):
Na
Na
>Al
Al
.③.原子序数为16号的元素Y对应的酸化学式为H2YO4,其中Y的化合价为
+6
+6
.④.原子序数为15的元素形成酸的化学式为H3PO4原子序数为16的元素形成酸的化学式为H2SO4,其中酸性较弱的是(用化学式表示)
H3PO4
H3PO4
.⑤.铝在实际生活中既能跟酸反应,也能与部分碱反应,如果将铝放入热的氢氧化钠水溶液中,将生成偏铝酸钠(NaAlO2)和氢气,试写出此反应的化学方程式
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
.分析:根据原子的序数来判断元素,结合信息从左到右元素的性质呈现特点为金属性逐渐减弱,非金属性逐渐增强;金属对应的碱的碱性逐渐减弱,非金属对应的酸的酸性逐渐增强来分析金属的活动性及酸的酸性强弱,利用化学式和常见元素的化合价来计算Y的化合价,利用反应物和生成物来书写化学反应方程式.
解答:解:①因X的原子序数为12,则为镁元素,属于金属元素,Y的原子序数为16,则为硫元素,属于非金属元素,故答案为:金属;非金属;
②原子序数为11的是钠元素,原子序数为13的是铝元素,根据从左到右元素的性质呈现特点为金属性逐渐减弱,则金属活动性Na>Al,故答案为:Na;Al;
③由化学式为H2YO4,H元素的化合价为+1价,O元素的化合价为-2价,根据化合物中正负化合价的代数和为0,则Y元素的化合价为0-(+1)×2-(-2)×4=+6,故答案为:+6;
④因P、S都是非金属元素,根据从左到右元素的性质非金属性逐渐增强,非金属对应的酸的酸性逐渐增强,则酸性H2SO4>H3PO4,故答案为:H3PO4;
⑤因铝放入热的氢氧化钠水溶液中,生成偏铝酸钠(NaAlO2)和氢气,反应为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
②原子序数为11的是钠元素,原子序数为13的是铝元素,根据从左到右元素的性质呈现特点为金属性逐渐减弱,则金属活动性Na>Al,故答案为:Na;Al;
③由化学式为H2YO4,H元素的化合价为+1价,O元素的化合价为-2价,根据化合物中正负化合价的代数和为0,则Y元素的化合价为0-(+1)×2-(-2)×4=+6,故答案为:+6;
④因P、S都是非金属元素,根据从左到右元素的性质非金属性逐渐增强,非金属对应的酸的酸性逐渐增强,则酸性H2SO4>H3PO4,故答案为:H3PO4;
⑤因铝放入热的氢氧化钠水溶液中,生成偏铝酸钠(NaAlO2)和氢气,反应为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
点评:本题考查学生对周期表中部分结构的认识和应用,学生应注意利用信息中性质的变化规律来分析解答,要求学生熟悉前20号元素的原子序数以便于进一步来分析解答问题.

练习册系列答案
相关题目
(2010?石狮市质检)小伟生日,妈妈做了很多菜,小伟发现妈妈将拌了“安多夫”粉的肉类加入食醋腌制时产生大量气泡,引发了极大的兴趣.
查阅资料:“安多夫”是一种嫩肉粉,可破坏肉质纤维结构,使肉质松软,其成分中含有碳酸氢(NaHCO3).小伟联想已经学过的碳酸钠(Na2CO3),其与碳酸氢钠比较,组成元素只相差一种元素氢元素,决定与化学兴趣小组的同学一道,对碳酸钠和碳酸氢钠的性质的异同点进行初步探究.
提出问题:碳酸钠和碳酸氢钠的性质有哪些相同点和不同点?
猜想1:碳酸氢钠溶液呈碱性.
进行实验1:
猜想2:碳酸氢钠能与盐酸反应
进行实验2:将气球中的碳酸氢钠粉末、碳酸钠粉末分别加入试管中:(如图),气球迅速胀大,说明碳酸氢钠能与盐酸发生化学反应.请写出碳酸氢钠与盐酸反应的化学反应方程式______.

交流与讨论1:通过上述两个实验结果,小伟同学得出结论:
碳酸氢钠与碳酸钠的化学性质相似.
其他同学对小伟的结论提出质疑,认为两者组成不完全相同,化学性质应有区别.于是,同学们设计并进
行以下甲、乙两个对比实验,实验装置如右图所示,请你参与,完成下列表格中的空白.
进行实验3:
交流讨论2:
(1)根据实验甲写出碳酸氢钠受热分解的化学方程式______ Na2CO3+H2O+CO2↑
查阅资料:“安多夫”是一种嫩肉粉,可破坏肉质纤维结构,使肉质松软,其成分中含有碳酸氢(NaHCO3).小伟联想已经学过的碳酸钠(Na2CO3),其与碳酸氢钠比较,组成元素只相差一种元素氢元素,决定与化学兴趣小组的同学一道,对碳酸钠和碳酸氢钠的性质的异同点进行初步探究.
提出问题:碳酸钠和碳酸氢钠的性质有哪些相同点和不同点?
猜想1:碳酸氢钠溶液呈碱性.
进行实验1:
| 实验操作 | 实验现象 | 实验结论 |
| 猜想是正确的 |
进行实验2:将气球中的碳酸氢钠粉末、碳酸钠粉末分别加入试管中:(如图),气球迅速胀大,说明碳酸氢钠能与盐酸发生化学反应.请写出碳酸氢钠与盐酸反应的化学反应方程式______.

交流与讨论1:通过上述两个实验结果,小伟同学得出结论:
碳酸氢钠与碳酸钠的化学性质相似.
其他同学对小伟的结论提出质疑,认为两者组成不完全相同,化学性质应有区别.于是,同学们设计并进
行以下甲、乙两个对比实验,实验装置如右图所示,请你参与,完成下列表格中的空白.
进行实验3:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验甲 | 取少量碳酸氢钠样品少许加入试管中,______. | 1.试管壁上有水珠. 2.______ | 反应生成了______和二氧化碳. |
| 实验乙 | 取碳酸钠样品少许重复实验甲的操作. | ______ | 碳酸钠受热不分解 |
(1)根据实验甲写出碳酸氢钠受热分解的化学方程式______ Na2CO3+H2O+CO2↑
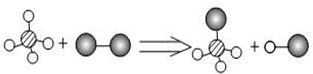 (2010?石狮市)已知某两种物质在光照条件下能发生化学反应,观察其微观示意图(如图),所得信息正确的是(说明:一种小球代表一种原子)( )
(2010?石狮市)已知某两种物质在光照条件下能发生化学反应,观察其微观示意图(如图),所得信息正确的是(说明:一种小球代表一种原子)( )