题目内容
【题目】某化学兴趣小组对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
Ⅰ.将3.0gKClO3与MnO2均匀混合加热
Ⅱ.将 xgKClO3与CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢。
I中反应表达式是_____;Ⅱ中x的值应为______。
(2)乙探究了影响过氧化氢分解速率的某种因素。实验数据记录如下:
过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
测量O2体积的装置是图甲中的________(填序号)。
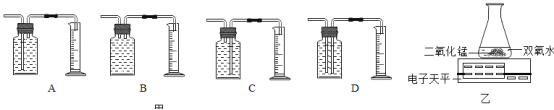
实验结论:在相同条件下,______,过氧化氢分解得越快。丙用图乙装置进行实验,通过比较_______也能达到实验目的。丁将盛有适量10%的过氧化氢溶液的试管加热,产生气泡明显增多。
实验结论:在相同条件下,_______,过氧化氢分解得越快。
【答案】![]() (文字表示式也可) 3.0 CD 过氧化氢洛液的浓度越大 相同时间,天平读数差值大小(无“差值”不给分) 温度越高
(文字表示式也可) 3.0 CD 过氧化氢洛液的浓度越大 相同时间,天平读数差值大小(无“差值”不给分) 温度越高
【解析】
(1)I中氯酸钾与二氧化锰混合制氧气同时生成氯化钾,反应表达式:![]() ;控制相同变量,则Ⅱ中x的值应该与I中氯酸钾的质量相等,x=3.0g;
;控制相同变量,则Ⅱ中x的值应该与I中氯酸钾的质量相等,x=3.0g;
(2)图C和D的集气瓶中,与量筒连接的玻璃导管,都伸入到了集气瓶底部,可以用排水法测量O2体积,故选:CD;
实验结论:由图表信息可知,在相同条件下,过氧化氢浓度越大,过氧化氢分解得越快。丙用图乙装置进行实验,通过比较相同时间,天平读数差值大小也能达到实验目的,丁将盛有适量10%的过氧化氢溶液的试管加热,产生气泡明显增多。
实验结论:在相同条件下,加热后产生气泡明显增多,说明温度越高,过氧化氢分解得越快。

【题目】某同学为了测定生铁样品中铁的质量分数,将60g 稀盐酸分3次加入到盛有4g 该样品的烧杯中(样品中只有铁与稀盐酸反应),所得数据如表,则下列说法中正确的是( )
实验次数 物质质量 | 第1次 | 第2次 | 第3次 |
加入稀盐酸的质量/g | 20 | 20 | 20 |
充分反应后剩余固体的质量 | 2.6 | 1.2 | 0.1 |
A.第1次和第2次产生氢气的质量不同
B.第2次和第3次剩余固体中均有铁
C.第3次充分反应后溶液中溶质只有FeCl2
D.生铁样品中铁的质量分数为97.5%
【题目】小明进行H2O2溶液制O2的实验探究。结合下列过程,回答有关问题。
(1)MnO2作催化剂,向5mL5%的H2O2溶液中加入少量MnO2,立即产生大量气泡。写出用H2O2溶液制备O2的文字表达式:________。
(2)向5mL5%的H2O2溶液中加入2滴一定浓度的 FeCl3溶液,立即产生大量气泡。
(查阅资料)FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-
(提出问题)那种微粒对H2O2溶液的分解起催化作用?
(提出假设)假设一:可能是H2O
假设二:可能是Fe3+
假设三:可能是_______。
(分析讨论)假设一不可能成立,理由是_______。
(实验探究)
步骤 | 实验操作 | 实验现象 | 结论 |
Ⅰ | 其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 | Na+,Cl-没有催化作用 |
Ⅱ | 其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 | __________ |
Ⅲ | 其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 | Fe3+有催化作用 |
(实验结论)假设_______成立,而假设一和另一种假设不成立。
(知识拓展)比较催化剂,从循环利用的角度分析,__(填化学式)更适合做该反应的催化剂。