题目内容
【题目】按要求用化学用语言填空.
(1)两个碳酸根离子________________ ;
(2)硫酸铁中的铁元素的化合价_________________ ;
(3)用盐酸去除铁锈(化学方程式)___________________________
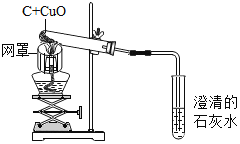
(4)工业上炼铁原理(化学方程式)___________________________________
【答案】2CO32- ![]() Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O 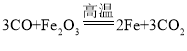
【解析】
(1)1个碳酸根离子带了2个单位的负电荷,在离子前的数字表示离子的个数。故答案为:2CO32-;
(2)该物质为硫酸铁,则铁元素为+3价。铁离子和硫酸根化合形成的物质为:Fe2(SO4)3,化合价应该标注在元素的正上方,且先写正负号后写数字。故答案为:![]() ;
;
(3)铁锈的主要成分是氧化铁,稀盐酸和氧化铁反应生成氯化铁和水。故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
(4)工业炼铁的原理是一氧化碳在高温下还原氧化铁,生成铁和二氧化碳。故答案为: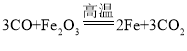 。
。

【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
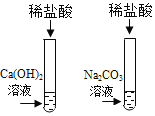
将反应后两只试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[假设与猜想]猜想一: NaCl
猜想二: NaCl 和CaCl2
猜想三: NaCl、Ca(OH)2 和HCl
猜想四:___________。
[讨论与交流]经讨论同学们一致认为猜想_________是错误的。原因是____________(用化学方程式解释)
[实验与结论]
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
取少量滤液于试管中,滴加适量_______________ | ______________________ |
[拓展与迁移]稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在_______________。