题目内容
 某化学兴趣小组的同学为了探究Mg、Cu、Fe的金属活动性顺序开展了一下以下探究活动.
某化学兴趣小组的同学为了探究Mg、Cu、Fe的金属活动性顺序开展了一下以下探究活动.(1)进行试验,获得结论.完成如下实验报告,并回答有关问题.
| 实验方案 | 实验现象 | 实验结论 | |
| 一 | 将Fe丝浸入CuSO4溶液中 | Fe丝表面有红色物质析出 | 金属活动性:Fe > > Cu(填“>”或“<”)该反应的反应类型属于置换 置换 反应. |
| 二 | 将Mg和Cu分别在空气中灼烧 | 发现 Mg Mg (填元素符号)能剧烈燃烧,而另一种不能 |
金属活动性:Mg > > Cu(填“>”或“<”) |
三 |
分别将Mg和Fe放入 稀硫酸 稀硫酸 (一种酸)溶液中,观察现象 |
观察到 Fe Fe (填元素符号)产生气泡的速度较慢 |
金属活动性顺序:Mg>Fe |
方法一是在相同时间内测量氢气体积的大小.若用如图所示装置测量,则接口c应与
a
a
(填“a”或“b”)相连.方法二是测定产生相同体积氢气时
所需的时间
所需的时间
.分析:(1)根据金属活动性顺序表及其应用分析.铁的活动性比铜强,铁可以置换出铜盐溶液中的铜;金属与盐反应生成另一种金属和另一种盐属于置换反应;镁的活动性比铜强,镁在空气中能燃烧而铜不能;镁和铁的活动性都在氢前,都能与酸反应,但镁的金属性比铁强,放出气泡较多;
(2)根据气体的密度和水的密度的关系分析接口的连接,进入量筒的水的体积就是收集到的氢气的体积,相同时间内收集的氢气越多产生氢气越快;产生相同体积氢气,所需的时间越短产生氢气越快,所需的时间越长产生氢气越慢.
(2)根据气体的密度和水的密度的关系分析接口的连接,进入量筒的水的体积就是收集到的氢气的体积,相同时间内收集的氢气越多产生氢气越快;产生相同体积氢气,所需的时间越短产生氢气越快,所需的时间越长产生氢气越慢.
解答:解:(1)方案一:铁可以置换出硫酸铜溶液中的铜,说明铁的活动性比铜强;铁与硫酸铜反应生成硫酸亚铁和铜,该反应由一种单质和化合物反应生成了另一种单质和另一种化合物,属于置换反应;
方案二:镁的活动性很强,在空气中镁就能剧烈燃烧而铜不能;
方案三:镁和铁的活动性都在氢前,都能与酸反应,但镁的活动性比铁强,放出气泡较多;
(2)由于氢气的密度小于水的密度,所以,氢气由b端通入水由a端流出,a端连接c端水流入量筒内,进入量筒的水的体积就是收集到的氢气的体积.相同时间内收集的氢气越多产生氢气越快;产生相同体积氢气,所需的时间越短产生氢气越快,所需的时间越长产生氢气越慢.
故答案为:(1)方案一>,置换; 方案二 Mg,>; 方案三 稀硫酸,Fe; (2)a,所需的时间.
方案二:镁的活动性很强,在空气中镁就能剧烈燃烧而铜不能;
方案三:镁和铁的活动性都在氢前,都能与酸反应,但镁的活动性比铁强,放出气泡较多;
(2)由于氢气的密度小于水的密度,所以,氢气由b端通入水由a端流出,a端连接c端水流入量筒内,进入量筒的水的体积就是收集到的氢气的体积.相同时间内收集的氢气越多产生氢气越快;产生相同体积氢气,所需的时间越短产生氢气越快,所需的时间越长产生氢气越慢.
故答案为:(1)方案一>,置换; 方案二 Mg,>; 方案三 稀硫酸,Fe; (2)a,所需的时间.
点评:本题考查学生对常见金属的活动性的比较.金属的活动性顺序,分析实验现象和结果都是中考的热点,应要引起重视.

练习册系列答案
相关题目
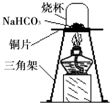 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.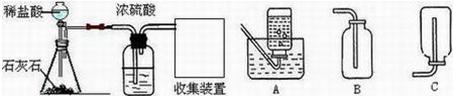
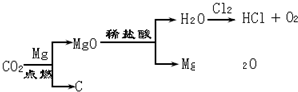
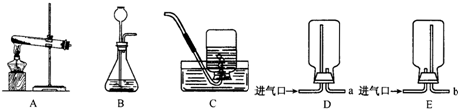
 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.