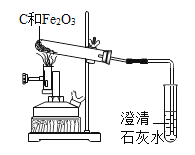
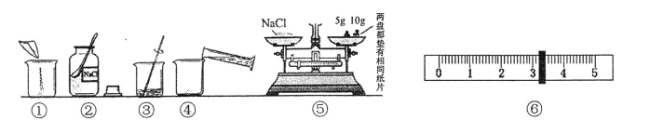
题目内容
【题目】在化学课上,老师带来一瓶未知溶液![]() 。
。
(提出问题1)![]() 是哪一类物质?
是哪一类物质?
(实验探究1)进行如下实验:
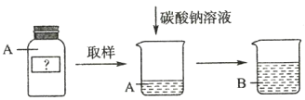
观察到烧杯中的现象是__________,说明![]() 是一种酸。
是一种酸。
(提出问题2)![]() 是哪一种酸?
是哪一种酸?
老师要求甲、乙同学从反应后的溶液![]() 分别展开探究。
分别展开探究。
(猜想假设)甲同学:![]() 是稀硫酸;乙同学:
是稀硫酸;乙同学:![]() 是稀盐酸。
是稀盐酸。
(实验探究2)
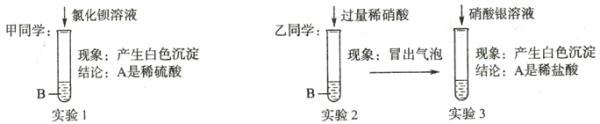
(评价交流)______(填“甲”或“乙”)同学的实验得出正确结论;另一位同学的结论错误的原因是__________。
(实验探究3)将实验1和实验3反应后的废液倒入同一烧杯中,充分反应后过滤,所得滤渣中一定含有______(填化学式),所得溶液中一定含有的离子是__________。发生反应的化学方程式为__________。
(归纳总结)通过乙同学的实验可以得出:选择试剂鉴别溶液中的待测离子时,如果待测溶液中含有干扰离子,则应在鉴别前,另选试剂将干扰离子除去。
【答案】有气泡冒出 乙 溶液![]() 中可能有碳酸根离子,生成的白色沉淀可能是碳酸钡
中可能有碳酸根离子,生成的白色沉淀可能是碳酸钡 ![]()
![]() 、
、![]() 、
、![]()
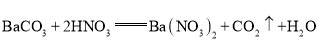
【解析】
[实验探究1]酸类物质能和碳酸钠反应生成二氧化碳而产生气泡,![]() 是一种酸,与碳酸钠溶液反应有气泡冒出;
是一种酸,与碳酸钠溶液反应有气泡冒出;
[评价交流]由于不确定![]() 中是稀硫酸还是稀盐酸,则
中是稀硫酸还是稀盐酸,则![]() 与碳酸钠反应后的溶液
与碳酸钠反应后的溶液![]() 中可能有碳酸钠,碳酸钠、硫酸钠都能与氯化钡反应生成白色沉淀,向
中可能有碳酸钠,碳酸钠、硫酸钠都能与氯化钡反应生成白色沉淀,向![]() 中加入氯化钡溶液也会产生白色沉淀,所以甲同学的结论错误;乙同学向
中加入氯化钡溶液也会产生白色沉淀,所以甲同学的结论错误;乙同学向![]() 中加过量的稀硝酸,排除碳酸钠的干扰,再滴加硝酸银溶液产生白色沉淀,说明
中加过量的稀硝酸,排除碳酸钠的干扰,再滴加硝酸银溶液产生白色沉淀,说明![]() 是稀盐酸,所以乙同学的结论正确;
是稀盐酸,所以乙同学的结论正确;
[实验探究3]实验1中的白色沉淀碳酸钡与实验3中的过量稀硝酸反应生成易溶于水的硝酸钡及二氧化碳、水,反应方程式为: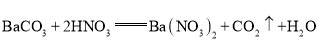 ,所以将实验1和实验3反应后的废液倒入同一烧杯中,充分反应后过滤,所得滤渣中一定含有
,所以将实验1和实验3反应后的废液倒入同一烧杯中,充分反应后过滤,所得滤渣中一定含有![]() ,滤液中一定有不参与反应的离子如
,滤液中一定有不参与反应的离子如![]() 、
、![]() ,以及经反应产生的
,以及经反应产生的![]() 。
。

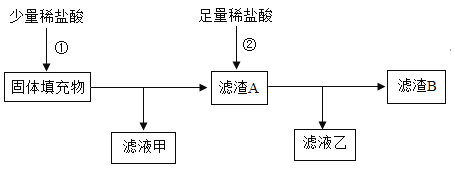
【题目】根据大量的实验总结,得出酸碱盐之间相互发生复分解反应的条件是生成物中有沉淀、气体或水。实验回顾如图:
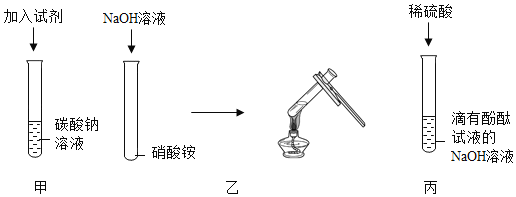
请回答
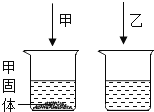
(1)甲实验有沉淀生成:加入的试剂是_____;
(2)乙实验有气体生成:化学方程式_____,检验气体的方法为_____;
(3)丙实验有水生成:氢氧化钠溶液中加入酚酞的作用是_____;
(4)依据复分解反应的条件可判断硫酸和氯化镁溶液不能发生反应。若想确认两种物质没有发生复分解反应,需要检验溶液中存在_____(写微粒符号)。
提出新问题:我们已经知道能发生复分解反应的两种盐通常是可溶的。有没有某些可溶性盐和难溶性盐能发生复分解反应?
查阅资料:
难溶性盐 | AgI | AgCl |
20℃时在水中的溶解度 | 3×107g | 1.5×104g |
颜色 | 黄 | 白 |
(5)实验取证:取少量硝酸银溶液于试管中,滴加过量的氯化钠溶液,有白色沉淀产生,继续加入少量KI溶液,白色沉淀转化为黄色沉淀,加入少量KI溶液后发生反应的化学方程式_____;
(6)结论某些可溶性盐和难溶性盐之间能发生复分解反应。从微观角度分析原因:反应朝着溶液中离子浓度(单位体积溶液中离子数目的多少)_____(填“减少”或“增大”)的方向进行。