题目内容
【题目】为判断某物质存在或某物质恰好完全反应,通常以特定物质的显色达到目,能显色的物质就称“指示剂”.如:用蓝色的石蕊试纸变红判断待测液显酸性;用淀粉溶液变蓝判断单质碘(I2)的存在: 已知:★SO2+I2+2H2O═H2SO4+2HI(无色溶液);
★常温下,碘微溶入水;
★5SO2+2H2O+KMnO4═K2SO4+2H2SO4+2MnSO4(无色溶液).
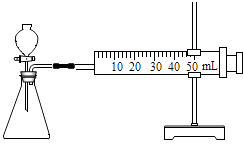
(1)工业上测量SO2 , N2 , O2混合气体的SO2含量用如图吸收装置(量气装置省略). 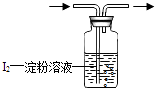
①混合气体通过图示吸收装置一定时间后,当溶液颜色由蓝色变为色时即可停止通气.此法适宜测SO2含量较(选填“低”或“高”)的混合气体.
②吸收装置内的I2的淀粉溶液一也可以用溶液代替作为指示剂.因为 .
(2)若用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应. 原盐酸中溶质的质量分数为 .
(3)试列式计算说明将该反应后的溶液转化为20℃时饱和溶液的一种简单方法(计算结果精确到0.1g).已知:20℃时氯化钠的溶解度为36.0g.
【答案】
(1)无;低;高锰酸钾;高锰酸钾溶液吸收一定量的SO2可由紫红色变为无色
(2)7.3%
(3)解:设该盐酸的溶质质量是x;生成的氯化钠质量是y.
NaOH + | HCl ═ | NaCl+H2O |
40 | 3605 | 58.5 |
16g×10% | X | y |
![]() ,x=1.46g
,x=1.46g
![]() ,y=2.34g
,y=2.34g
以盐酸的溶质质量分数为 ![]() ×100%=7.3%;
×100%=7.3%;
由于该溶液在20℃时不饱和所以可采用加溶质的简便办法使其转化成饱和溶液,原溶液质量是20g+16g=36g;
设加入溶质的质量是z,则有 ![]() ×100%=
×100%= ![]() ×100%
×100%
则z≈9.8g
【解析】解:(1)①碘的淀粉溶液呈蓝色,由于SO2+I2+2H2O═H2SO4+2HI(无色溶液)可知该溶液由蓝色变成无色时该反应恰好完成,此时应该停止通入气体,通入过量气体会使测量结果不准确,常温下,碘微溶入水,所以碘的淀粉溶液吸收二氧化硫的量较小,故该装置吸收二氧化硫的量较小,所以此法适宜测SO2含量较低的混合气体.②因为紫红色高锰酸钾的溶液通入二氧化硫时会发生5SO2+2H2O+KMnO4═K2SO4+2H2SO4+2MnSO4(无色溶液)的反应,溶液现象由紫红色变成无色,所以也可采用高锰酸钾溶液代替碘的淀粉溶液完成该实验.(2)由题干可知10.0%的氢氧化钠溶液16.0g和20.0g盐酸恰好完全反应,因此可通过反应的方程式对盐酸的溶质质量分数进行计算,也可计算出生成的氯化钠质量;所以答案是:(1)①无;低;②高锰酸钾;高锰酸钾溶液吸收一定量的SO2可由紫红色变为无色;(2)①7.3%②可向溶液中加入9.8g氯化钠.
【考点精析】认真审题,首先需要了解饱和溶液和不饱和溶液相互转变的方法(饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂),还要掌握根据化学反应方程式的计算(各物质间质量比=系数×相对分子质量之比)的相关知识才是答题的关键.