题目内容
用氢气做还原剂在一定条件下还原8克氧化铜,如果完全反应,则单质铜的质量是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:利用氢气还原氧化铜制取铜的化学方程式和已知氧化铜的质量,列出比例式,就可计算出能够制得铜的质量.
解答:解:设能够制得铜的质量是x,
CuO+H2
Cu+H2O
80 64
8g x
=
x=6.4g
答案:单质铜的质量是6.4g
CuO+H2
| ||
80 64
8g x
| 80 |
| 64 |
| 8g |
| x |
x=6.4g
答案:单质铜的质量是6.4g
点评:本题是有关化学方程式的简单计算.解题时要注意格式,计算要细心.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
工业酒精中常含有甲醇(CH3OH),误食后能使人眼睛失明,甚至死亡.下列有关甲醇的说法不正确的是( )
| A、甲醇是由1个碳原子、2个氢原子、1个氧原子构成 |
| B、甲醇中碳、氢、氧三种元素的质量比为3:1:4 |
| C、24g甲醇中含碳元素8g |
| D、甲醇中氧元素的质量分数为50% |
煤燃烧产生的废气中含有SO2,用NaOH、Na2SO3溶液可将90%以上的SO2吸收.涉及的反应有
①2NaOH+SO2═Na2SO3+H2O ②Na2SO3+SO2+H2O═2NaHSO3 ③NaHSO3+NaOH═Na2SO3+H2O
下列说法中,不正确的是( )
①2NaOH+SO2═Na2SO3+H2O ②Na2SO3+SO2+H2O═2NaHSO3 ③NaHSO3+NaOH═Na2SO3+H2O
下列说法中,不正确的是( )
| A、反应②是化合反应 |
| B、可循环使用的物质是Na2SO3 |
| C、NaHSO3中硫元素的化合价是+6 |
| D、煤脱硫后燃烧可防止煤燃烧产生SO2 |
下列物质属于化学性质的是( )
| A、水在4℃时密度为1g/cm3 |
| B、镁条可以在空气中燃烧 |
| C、胆矾是蓝色固体 |
| D、汽油能挥发 |
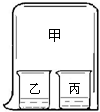 如图所示,在小烧杯乙和丙内分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙.下列有关实验现象补充完整.
如图所示,在小烧杯乙和丙内分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙.下列有关实验现象补充完整.