题目内容
人体缺乏维生素C可能得坏血病,维生素C的化学式是C6H8O6,在新鲜的水果、蔬菜中都含量较高,探究小组测定了某品牌橙汁的维生素C的含量.过程如下:取20.00g橙汁用含碘1.00%的碘溶液与其反应,恰好反应时消耗碘溶液25.40g(反应方程式:C6H8O6+I2═C6H6O6+2HI)
求:(1)维生素C分子中氧元素的质量分数是______(保留2位小数)
(2)橙汁中维生素C的质量分数是多少?(列式计算)
解:(1)维生素C分子中氧元素的质量分数是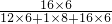 ×100%=54.55%;
×100%=54.55%;
(2)设20.00g橙汁含维生素C的质量为x
C6H8O6+I2=C6H6O6+2HI
176 254
x 25.40g×1.00%
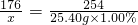 ,
,
x=0.176g;
维生素C的质量分数=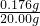 ×100%=0.88%.
×100%=0.88%.
故答案为:(1)54.55%;(2)橙汁中维生素C的质量分数为0.88%
分析:(1)依据维生素C的化学式进行计算即可;
(2)根据化学方程式和恰好完全反应时消耗碘的质量,列出比例式,就可计算出20.00g橙汁含维生素C的质量;然后根据质量分数公式计算即可;
点评:本题主要考查学生运用化学式及化学方程式进行计算的能力.根据化学方程式和其中一种物质的质量,可以求出所需物质的质量
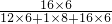 ×100%=54.55%;
×100%=54.55%;(2)设20.00g橙汁含维生素C的质量为x
C6H8O6+I2=C6H6O6+2HI
176 254
x 25.40g×1.00%
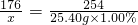 ,
,x=0.176g;
维生素C的质量分数=
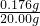 ×100%=0.88%.
×100%=0.88%.故答案为:(1)54.55%;(2)橙汁中维生素C的质量分数为0.88%
分析:(1)依据维生素C的化学式进行计算即可;
(2)根据化学方程式和恰好完全反应时消耗碘的质量,列出比例式,就可计算出20.00g橙汁含维生素C的质量;然后根据质量分数公式计算即可;
点评:本题主要考查学生运用化学式及化学方程式进行计算的能力.根据化学方程式和其中一种物质的质量,可以求出所需物质的质量

练习册系列答案
相关题目