题目内容
【题目】某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
Ⅰ.定性探究
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
(1)【猜想与假设】
猜想Ⅰ:溶液中的溶质只有;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl。
(2)经过讨论,同学们直接得出不合理的猜想是哪一种并说出理由:。
为了验证余下的哪一种猜想是正确的,同学们又做了以下实验。
(3)【进行实验】研究
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | 溶液不变色 | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钠 | 有气泡产生 | 猜想正确 |
(4)操作②有气泡生成的化学方程式为。
(5)下列曲线能够表示所做实验中溶液pH变化趋势的是 (填序号)。
A.滴加盐酸的质量 
B.滴加盐酸的质量 
C.滴加盐酸的质量 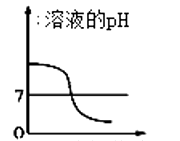
D.滴加盐酸的质量 
(6)【反思交流】
要使烧杯内溶液的溶质只含CaCl2 , 需要除去杂质,其中的一种方法是向烧杯中加入过量的 , 然后过滤。
(7)Ⅱ.定量探究
兴趣小组同学想对本地化工厂排放废水中的HCl含量进行了测定(不含其他酸性物质)。取废水5 g,用质量分数为2%的氢氧化钙溶液进行中和,如下图所示。请你计算废水中HCl的质量分数。(写出具体的计算过程)
【答案】
(1)CaCl2
(2)猜想Ⅳ,盐酸和氢氧化钙相互反应。不能共存
(3)猜想Ⅱ正确
(4)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(5)C
(6)碳酸钙/石灰石/大理石
(7)解:设废水中HCl的质量为x,
37g氢氧化钙溶液中含溶质Ca(OH)2的质量为37g×2%=0.74g
Ca(OH)2+ | 2HCl=CaCl2+2H2O |
74 | 73 |
0.74g | x |
![]()
x=0.73g
废水中HCl的质量分数为 ![]() ×100%=14.6%
×100%=14.6%
答:废水中HCl的质量分数为14.6%。
【解析】【猜想与假设】(1)反应可能是一种物质完全反应,另一种物质有剩余:若氢氧化钙过量,则含有氢氧化钙和氯化钙;若盐酸过量,则含有盐酸和氯化钙;也可能是恰好反应:只有氯化钙;故填:CaCl2;(2)因为稀盐酸与氢氧化钙在溶液中不能共存,所以猜想四不合理;(3)再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钠,有气泡产生,则证明剩余溶液中含有HCl,则猜想Ⅱ成立,猜想Ⅰ不成立;(4)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;(5)氢氧化钙溶液显碱性,pH>7,逐渐加入盐酸,随着反应进行,碱性逐渐减弱至中性,后盐酸过量,pH<7,故选:C;(6)要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,即除去稀盐酸,可加入过量的碳酸钙(或石灰石或大理石),碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,然后过滤;
根据反应后物质成分除生成物一定存在外,还要证明反应物是否有剩余分析;根据化学方程式计算分析,利用方程式进行计算时,要先写出有关反应方程式,根据方程式量的关系找出相关物质的相对质量比,再从题中找出已知物质的质量,利用相对质量比与实际质量比相等利出比例式求解,注意溶液之间的反应,参加反应的物质为溶液中的溶质,代入方程式中的质量必须是参加反应或生成的纯净物的质量。

【题目】.学好化学要会归纳和总结,下列归纳错误的是( )
A.化学常识 | B.生活常识 |
硬水含有较多可溶性钙镁化合物的水 合金混合物 | 甲醛浸泡动物标本使标本能长期保存 小苏打是治疗胃酸过多症的一种药剂 |
C.物质的性质与用途 | D.吸热与放热现象 |
生石灰用作干燥剂 钨丝用于制作白炽灯灯丝 | 吸收热量氢氧化钠固体溶于水 放出热量硝酸铵固体溶于水 |
A.AB.BC.CD.D
【题目】A、B、C、D表示四种物质,其微观示意图见下表。A和B在一定条件下反应生成C和D,
物质 | A | B | C | D |
|
微观示意图 |
|
|
|
|
(1)这四种物质中,由原子直接构成的物质是_________(填化学式)。A物质名称是___________。该反应的化学方程是_____________________。
(2)若有64gB完全参加反应,则生成C的质量为____________g。
(3)从微观的角度揭示化学反应的本质是_____________________________。
(4)上述反应中,一定发生改变的是_______________(填编号)。
①原子种类 ②分子种类 ③原子个数 ④原子质量