题目内容
将一定质量的碳酸钠粉末溶于400克水中配制成溶液,取一半该溶液,向其中加入20%的盐酸若干克,恰好反应完全,放出气体的质量为22克.试计算:
(1)碳酸钠溶液的总质量;
(2)反应后所得溶液中溶质的质量分数.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x y z 22g

解之得 x=53g
y=36.5g
z=58.5g
碳酸钠溶液的总质量=53g×2+400g=506g
反应消耗稀盐酸的质量=
 =182.5g
=182.5g反应后所得溶液中溶质的质量分数=
 ×100%≈14.1%
×100%≈14.1%答:(1)Na2CO3溶液的总质量为506克;
(2)反应后所得溶液中溶质的质量分数为14.1%
分析:根据溶液的均一性,取一半该溶液,即由生成的22g二氧化碳所计算得到的碳酸钠仅为原粉末质量的一半;
恰好完全反应,所以,反应后所得溶液为氯化钠溶液,计算出反应生成氯化钠的质量与溶液质量比.
点评:因为取一半的溶液,即有200g水,53gNa2CO3,182.5g稀盐酸溶液,生成22g二氧化碳逸出,故根据质量守恒定律,反应物物溶液的质量=200g+53g+182.5g-22g=413.5g.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案回答下列问题。
⑴铁在食品防腐上有重要的作用。为防止月饼变质,常在内包装中放入一小包防腐剂,其主要成分是铁粉。铁粉的作用是 。
⑵将锌粉加入到由AgNO3和Cu(NO3)2组成的一定质量的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为__________________,滤液中的溶质是___________________。
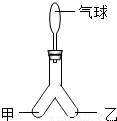
⑶用如图所示装置进行下列实验,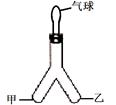
向“人”字型管的甲、乙两端分别装入适量表中所示物质,并进行相应操作,填写下表。
| 甲中的物质 | 乙中的物质 | 操 作 | 现 象 |
| 饱和石灰水 | 浓硫酸 | 盖上塞子,较长时间后 | ① |
| 碳酸钠溶液 | 盖上塞子,倾斜装置,使乙中液体流入甲中 | ② | |
| 少量碳酸钙固体 | 向乙中滴入少量稀盐酸后盖上塞子 | ③ | |
| 底部有少量KNO3固体的KNO3溶液 | 将甲、乙两端同时放入热水中 | ④ | |
| ⑤甲中 | 乙中 | 倾斜装置,使乙中液体流入甲中 | 甲中有无色气泡产生 |
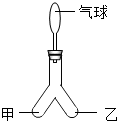 回答下列问题.
回答下列问题.
(1)铁在食品防腐上有重要的作用.为防止月饼变质,常在内包装中放入一小包防腐剂,其主要成分是铁粉.铁粉的作用是______.
(2)将锌粉加入到由AgNO3和Cu(NO3)2组成的一定质量的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为______,滤液中的溶质是______.
(3)用如图所示装置进行下列实验,向“人”字型管的甲、乙两端分别装入适量表中所示物质,并进行相应操作,填写下表.
| 甲中的物质 | 乙中的物质 | 操 作 | 现 象 |
| 饱和石灰水 | 浓硫酸 | 盖上塞子,较长时间后 | ①______ |
| 碳酸钠溶液 | 盖上塞子,倾斜装置,使乙中液体流入甲中 | ②______ | |
| 少量碳酸钙固体 | 向乙中滴入少量稀盐酸后盖上塞子 | ③______ | |
| 底部有少量KNO3固体的KNO3溶液 | 将甲、乙两端同时放入热水中 | ④______ | |
| ⑤甲中 ______ | 乙中 ______ | 倾斜装置,使乙中液体流入甲中 | 甲中有无色气泡产生 |
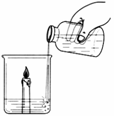 某活动小组的同学对碳酸钠与稀盐酸反应进行了下列探究:
某活动小组的同学对碳酸钠与稀盐酸反应进行了下列探究:
【探究一】向放有一支燃着的蜡烛的烧杯中加适量碳酸钠和盐
酸(如图所示):
(1)蜡烛燃烧变化的现象是: 。
(2)根据该实验现象推测碳酸钠与盐酸反应产生的气体可用于 (写出用途)。
【探究二】利用碳酸钠与盐酸的反应,可否用于验证质量守恒定律进行了探究,实验如下:
|
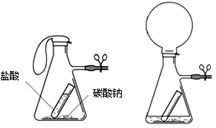 如右图所示,在(吸滤)瓶中加入适量的碳酸钠粉
如右图所示,在(吸滤)瓶中加入适量的碳酸钠粉 末,在小试管中加入盐酸。将小试管放入吸滤瓶中,
并用止水夹夹住支管处的橡皮管。称量整个装置的
质量,记录读数。将吸滤瓶倾斜,使小试管中的盐
酸倾倒入瓶中,与碳酸钠粉末反应。可观察到如图二
所示的现象。再次称量整个装置的质量,记录读数。
两次读数 (填“是”或“否”)相等。理由是 。
【探究三】碳酸钠与盐酸反应后剩余溶液的成分探究(假设二氧化碳已完全放出,杂质溶于水,不参加反应且呈中性)。甲、乙两同学分析认为剩余溶液中一定含有氯化钠,可能有盐酸或碳酸钠。为验证是否含有盐酸,他们采用了不同方法进行实验,得到了相同的结论。
查找资料:氯化钠溶液呈中性
| 实验操作 | 实验现象 | 结论 | |
| 甲 | 取样于试管中,滴加 试液[ | 试液变红 | 有盐酸 |
| 乙 | 取样于试管中,逐滴滴加碳酸钠溶液[ |
|
【探究四】某兴趣小组同学向盛有6.0g纯碱样品的烧杯里加入40.0g盐酸,实验测定完全反应后烧杯中剩余物的质量为43.8g,且溶液显酸性。(假设纯碱样品中的杂质不与盐酸反应)求:
(1)产生的二氧化碳的质量为 g。
(2)纯碱样品中碳酸钠的质量(写出计算过程)。
(1)铁在食品防腐上有重要的作用.为防止月饼变质,常在内包装中放入一小包防腐剂,其主要成分是铁粉.铁粉的作用是 .
(2)将锌粉加入到由AgNO3和Cu(NO3)2组成的一定质量的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为 ,滤液中的溶质是 .
(3)用如图所示装置进行下列实验,向“人”字型管的甲、乙两端分别装入适量表中所示物质,并进行相应操作,填写下表.
| 甲中的物质 | 乙中的物质 | 操 作 | 现 象 |
| 饱和石灰水 | 浓硫酸 | 盖上塞子,较长时间后 | ① |
| 碳酸钠溶液 | 盖上塞子,倾斜装置,使乙中液体流入甲中 | ② | |
| 少量碳酸钙固体 | 向乙中滴入少量稀盐酸后盖上塞子 | ③ | |
| 底部有少量KNO3固体的KNO3溶液 | 将甲、乙两端同时放入热水中 | ④ | |
| ⑤甲中 | 乙中 | 倾斜装置,使乙中液体流入甲中 | 甲中有无色气泡产生 |
 (2012?丰台区二模)回答下列问题.
(2012?丰台区二模)回答下列问题.