题目内容
【题目】(2017金华改编)为了测定一瓶未密封保存的NaOH固体中NaOH的质量分数,小科采用沉淀法进行如下操作:①取15 g样品于烧杯中,加足量水配成溶液;②在样品溶液中加入足量的BaCl2溶液;③待反应完全后,过滤。有关数据记录如下表:
反应前 | 反应后 | |
烧杯和样品溶液总质量/g | 加入的氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
95 | 65 | 140.3 |
请计算:
(1)反应共生成沉淀________g。
(2)原样品中NaOH的质量分数。(结果精确到0.1%)
【答案】(1)19.7(2)29.3%
【解析】
解:设样品中Na2CO3的质量为x
Na2CO3+BaCl2=== BaCO3↓+2NaCl
106 197
x 19.7 g
![]() =
=![]() x=10.6 g
x=10.6 g
原样品中NaOH的质量为15 g-10.6 g=4.4 g
原样品中NaOH的质量分数为![]() ×100%≈29.3%
×100%≈29.3%
答:原样品中NaOH的质量分数约为29.3%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
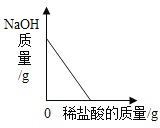
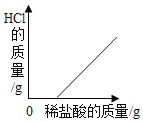
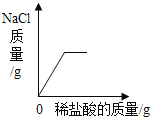
小学生10分钟应用题系列答案【题目】如图是物质甲与足量物质乙发生化学反应的过程中固体总质量随时间的变化趋势,下列所给物质间的反应符合坐标曲线的是( )
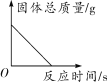
选项 | 物质甲 | 物质乙 |
A | 木炭 | 氧化铜 |
B | 铁丝 | 氧气 |
C | 碳酸钙 | 盐酸 |
D | 铜片 | 硝酸银溶液 |
A.AB.BC.CD.D
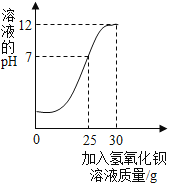
【题目】某化学兴趣小组利用稀盐酸和澄清石灰水展开“酸碱中和反应”的实验探究活动。请你参与他们的实验活动,并回答相关问题
(提出问题Ⅰ)稀盐酸和澄清石灰水能否发生反应?
(实验1)小明取一定量的稀盐酸,测得其pH=2,然后向其中加入一定量的澄清石灰水后,测得混合溶液的pH=3,于是得出“稀盐酸和澄清石灰水发生了中和反应”的结论。
测定溶液pH的方法是:将pH试纸放在玻璃片上,___,将试纸显示的颜色与标准比色卡比较。
小刚认为,小明的实验方案不能证明二者发生了中和反应,理由是___。
(实验2)小刚取稀盐酸于试管中,加入一定量的澄清石灰水,得到溶液X,再加入适量铁粉,观察到___,证明稀盐酸和澄清石灰水发生了反应。
稀盐酸和澄清石灰水反应的化学方程式为___。
(提出问题Ⅱ)溶液X中溶质的成分是什么?
猜想一:只有CaCl2;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和HCl
小组同学为验证猜想二,进行了如下实验(查阅资料显示CaCl2溶液显中性)
实验操作 | 实验现象 | 实验结论 | |
实验3 | 取适量溶液X于试管中,滴加紫色石蕊溶液 | ___ | 猜想二成立 |
实验4 | 取适量溶液X于试管中,滴加Na2CO3溶液 | 产生白色沉淀 | 猜想二成立 |
小明认为实验4中产生白色沉淀,并不能证明猜想二成立,理由是____。
请你另选一种试剂,设计合理的方案,当观察到与实验4相同的现象时,证明猜想二成立。你的实验原理是___(用化学方程式表示)。