题目内容
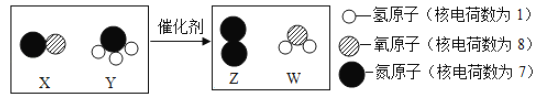
【题目】在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。某课外兴趣小组对生成物中碳的氧化物种类等问题进行了如下探究:
(提示)①CO2+2NaOH=Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水;④氧化铁为红色粉末,铁粉为黑色固体。
(提出问题)生成物中有哪几种碳的氧化物?
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有CO2 | ______ |
(设计实验)兴趣小组同学设计了如下实验:
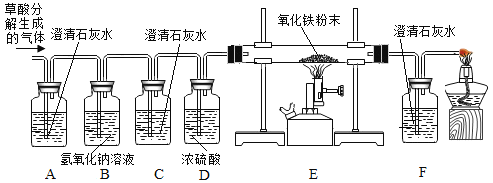
(实验探究)
(1)观察到_____装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。该装置中发生反应的化学方程式为____________。C装置中作用是________
(2)观察到:①C装置中_________________ ,F装置中_____________;
②E装置中出现________的现象。
上述现象都能分别证明草酸分解的气体中含有CO。其中E装置中发生反应的化学方程式为_________。
(实验结论)猜测3成立。
(拓展与反思)
(1)装置末端酒精灯的作用是____;
(2)若B装置没有把二氧化碳气体完全吸收,可能的一条原因是_______;
【答案】CO和CO2 A CO2+Ca(OH)2=CaCO3↓+H2O 检验二氧化碳是否被完全吸收 澄清石灰水不变浑浊 澄清的石灰水会变浑浊 红色粉末变成黑色 3CO+Fe2O3![]() 2Fe+3CO2 点燃尾气中一氧化碳,防止污染空气 氢氧化钠溶液的浓度太小
2Fe+3CO2 点燃尾气中一氧化碳,防止污染空气 氢氧化钠溶液的浓度太小
【解析】
[提出问题]碳的氧化物可能是一氧化碳,或二氧化碳,或一氧化碳和二氧化碳;故可根据猜想1、2的内容,推测猜想3的内容;故填:CO和CO2;
[实验探究](1)如果生成的气体中含有二氧化碳,通过A装置时,澄清的石灰水会变浑浊;C装置中作用是检验二氧化碳是否被完全吸收.故填:A;CO2+Ca(OH)2=CaCO3↓+H2O;检验二氧化碳是否被完全吸收;
(2)C装置中澄清石灰水不变浑浊,说明原有的二氧化碳已经被完全吸收;E装置中红色粉末变成黑色,说明氧化铁被还原;F中澄清石灰水变浑浊,说明有二氧化碳生成,说明还原气是CO;E中发生的反应是一氧化碳和氧化铁在高温条件下生成铁和二氧化碳;
故答案为:①澄清石灰水不变浑浊;澄清的石灰水会变浑浊;②红色粉末变成黑色;3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
[拓展与反思]
(1)为防止一氧化碳污染空气,装置末端酒精灯可以点燃尾气CO;故填:点燃尾气中一氧化碳,防止污染空气;
(2)若B装置没有把二氧化碳气体完全吸收,可能的原因是氢氧化钠溶液的浓度太小,故填:氢氧化钠溶液的浓度太小。

 阅读快车系列答案
阅读快车系列答案