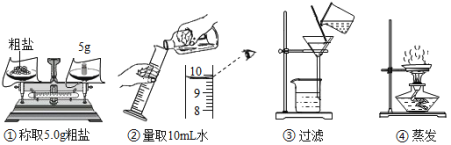
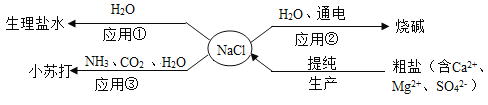
题目内容
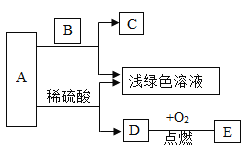
【题目】某化学兴趣小组的同学想从含有Al2(SO4)3、CuSO4 的废液中回收金属铜,设计流程如图:
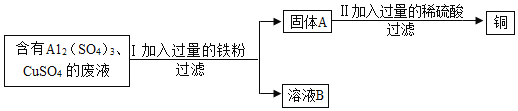
(1)Ⅰ中有关反应的化学方程式为_____。
(2)溶液B中所含的溶质是_____(填化学式)。
(3)Ⅱ中加入过量的稀硫酸的目的是_____。
(4)过程Ⅰ、Ⅱ中涉及反应的基本类型为_____。
【答案】Fe+CuSO4═FeSO4+Cu A12(SO4)3、FeSO4 除去固体A中的铁 置换反应
【解析】
(1)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═FeSO4+Cu;故填:Fe+CuSO4═FeSO4+Cu。
(2)铁会置换出硫酸铜中的铜,不会置换出硫酸铝中的铝,所以固体A是Cu、Fe,溶液B中所含的溶质是A12(SO4)3、FeSO4;故填:A12(SO4)3、FeSO4。
(3)过量的铁会与稀硫酸反应,所以II中加入过量的稀硫酸的目的是除去除去固体A中的铁;故填:除去固体A中的铁。
(4)过程Ⅰ、Ⅱ中涉及反应均为单质和化合物反应生成另一种单质和化合物,其反应的基本类型为置换反应;故填:置换反应。

【题目】如表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如下图所示的两个溶解实验。
物质/溶解度/g/温度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
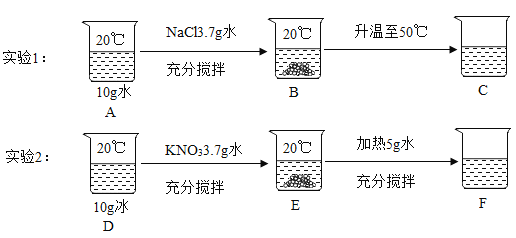
(1)由表格数据可知,溶解度随温度升高变化显著的物质是_____(选填“NaCl”或“KNO3”)。
(2)上述溶液中属于饱和溶液的是_____(填 A-F 序号)。
(3)BCEF 溶液中溶质质量分数由大到小的关系是_____(用“<”、“>”、“=”表示)
(4)关于图中有关说法不正确的是_____。
A B烧杯的溶液还可以溶解硝酸钾固体
B 将20℃时硝酸钾的不饱和溶液转化为饱和溶液的方法:蒸发溶剂或升高温度
C 氯化钠中混有少量的硝酸钾可以用蒸发结晶的方法除去
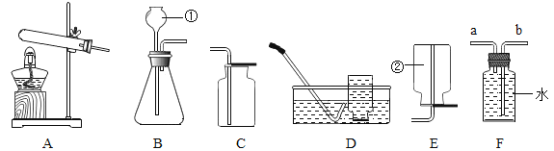
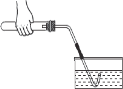
【题目】某同学在做二氧化锰催化氯酸钾分解的实验时,不小心将黑色的氧化铜当作二氧化锰与氯酸钾混合加热,用排水法收集,发现集气瓶中气泡的产生速率加快了。难道氧化铜对氯酸钾的分解也有催化作用?该同学展开如下探究:
(提出问题)氧化铜对氯酸钾的分解是否有催化作用?
(设计实验)
实验组 | 实验步骤 | 测量数据 |
① | 将 3.0 g 氯酸钾放在试管中加热,用排水法收集生成的气体 | |
② | 将 3.0 g 氯酸钾与 1.0 g 二氧化锰均匀混合加热,用排水法收集生成的气体 | |
③ | 将 x g 氯酸钾与 1.0 g 氧化铜均匀混合加热,用排水法收集生成的气体 |
(1)写出实验室加热氯酸钾和二氧化锰的混合物制氧气的化学方程式_____。
(2)实验③中 x 的数值为_____,测量数据为_____。
(实验结论)
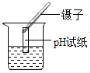
(3)经验证,氧化铜可代替二氧化锰催化氯酸钾分解。将实验③完全反应后的固体加水溶解、过滤、_____,若称量得到 1.0 g 黑色粉末(假设氯酸钾完全反应),再将黑色粉末和氯酸钾混合加热,集气瓶中的现象与实验③_____(填“相同”或“不同”)。
(4)实验室还可以用过氧化氢溶液为原料制取氧气,与以氯酸钾为原料制取氧气相比,用过氧化氢溶液作原料的优点是_____(写一点即可)。某同学查阅资料发现氧化铜也能催化过氧化氢溶液分解。小组同学为了比较二氧化锰和氧化铜对过氧化氢溶液的催化效果,利用数字化仪器测得室温下质量相同的两种物质分别与 5 mL 5%的过氧化氢溶液在两个相同的密闭容器内混合时装置内压强的变化过程。
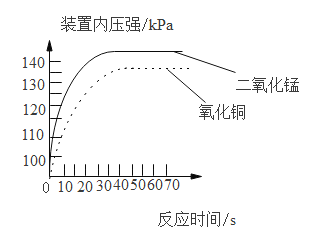
(5)由图像可知:常温下,_____对过氧化氢的分解催化效果更好。
(6)小明推测两条曲线最终将合并在一起,请你说出他的理由_____。