题目内容
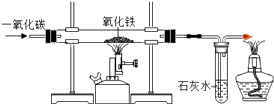
【题目】t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.下列说法正确的是( )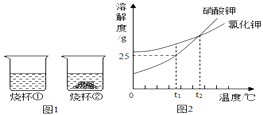
A.烧杯①中的溶液一定未达到饱和状态
B.烧杯②中溶解的溶质是氯化钾
C.蒸发一定量的水,两烧杯中都一定有固体析出
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
【答案】D
【解析】A、 烧杯①加入的硝酸钾没有具体质量, 烧杯①中的溶液饱和与不饱和状态不确定,故A错误;A不符合题意;
B、烧杯②中溶解的溶质应该是硝酸钾,t1℃时硝酸钾溶解度小于氯化钾,有可能是硝酸钾没有溶解完,故B错误;B不符合题意;
C、根据题中信息不能确定①溶液是否饱和, 蒸发一定量的水,烧杯②是饱和溶液一定有固体析出,烧杯①若是饱溶液一定有固体析出,若是不饱和溶液就不一定有固体析出,故C错误;C不符合题意;
D、等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,将温度升高到t2℃,硝酸钾和氯化钾均全部溶解,溶质和溶剂的量完全相等,溶液的组成相同,两烧杯内溶液中溶质的质量分数相等,故D正确。D符合题意;
故答案为:D
饱和溶液是指的是在一定温度下,一定剂量的溶剂里面,不能继续溶解溶质,也就意味着溶液的浓度不变。同一温度下,溶解度大的物质比溶解度小的物质更易完全溶解;蒸发等量的水,要析出的晶体量相等,必须是蒸发前的饱和溶液的质量相等;溶液升温后,只要溶液的组成不变,溶质的质量分数就应该不变;

【题目】分类、类比是初中化学常用的学习方法.请回答下列问题:
(1)初中化学有许多实验中都用到了水,但是用水作用是不同的,将下列实验中的B与①(填字母)归为一类,理由是②
|
|
|
|
A | B | C | D |
(2)1865年,俄国学者贝开托夫(Beketob)在实验的基础上,根据金属和金属离子间互相置换能力的大小,以及金属跟酸、水等反应的剧 烈程度,首先确定了金属活动性顺序,在这个顺序里包括了氢.在金活动性顺序中活动性越强,其金属的还原性也越强.确定金属的活动性也可以根据元素在元素周期表中的位置判断,如图是元素周表的一部分.请回答下列问题. 
金属活动性顺序为:K Ca Na Mg…
请推断金属铍的佥属活动性比金属镁的活动性①(填“强”或“弱”);金属锂的还原性比金属镁的还原性②(填“强”或“弱”).