题目内容
【题目】碳酸氢钠是一种重要的盐类物质,在生活中用途广泛。小红同学设计实验对碳酸氢钠的性质进行了探究。请你参与她的探究活动。
(探究实验1)碳酸氢钠溶液的酸碱性。
(实验方案)取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡。现象:溶液变成浅红色。 结论: ① 。
(探究实验2)能与酸反应。
(实验方案)取少量该固体加入试管中,滴加稀盐酸。现象: ② 。反应的化学方程式为: ③ 。
(探究实验3)碳酸氢钠的热稳定性。
(实验方案)设计实验装置如图,并进行实验。
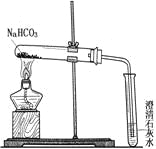
现象: 试管口有水珠出现,澄清石灰水变浑浊。充分加热后,试管中留下白色固体。
结论:碳酸氢钠受热有二氧化碳.水和白色固体生成。
请你帮小红设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH。(所选试剂不能用酸)
步骤: ④ ;
现象: ⑤ 。
试写出碳酸氢钠受热发生反应的化学方程式:⑥ 。
(拓展应用)根据以上探究,请说出碳酸氢钠在日常生活中的一种用途: ⑦ 。
【答案】(7分) ①碳酸氢钠溶液呈碱性(说明:回答“碳酸氢钠呈碱性”或“碱性”不给分)
②产生气泡
③NaHCO3+HCl = NaCl+H2O+CO2↑
④取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水
⑤溶液变浑浊(说明:根据④设计方案的不同⑤的现象也不同,只要合理均可给分)
⑥2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
⑦治疗胃酸的药物(或用作发酵粉)
【解析】
试题碳酸氢钠溶液的酸碱性。取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡。现象:溶液变成浅红色。 结论:碳酸氢钠的溶液显示碱性,取少量该固体加入试管中,滴加稀盐酸。现象:有气泡冒出,方程式为NaHCO3+HClNaCl+H2O+CO2↑,设计实验装置如右图,并进行实验。现象: 试管口有水珠出现,澄清石灰水变浑浊,充分加热后,试管中留下白色固体。结论:碳酸氢钠受热有二氧化碳.水和白色固体生成。设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH。(所选试剂不能用酸) 步骤:取少量固体放入试管内,加水溶解,滴入氯化钙溶液,振荡。现象:有白色沉淀产生。说明是碳酸钠不是氢氧化钠,因为氢氧化钠不会和氯化钙反应,碳酸氢钠在日常生活中的一种用途:治疗胃酸过多等。

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案