题目内容
【题目】 在做电解水实验时,常在水中加入氢氧化钠来增强溶液的导电性,但氢氧化钠本身不会发生化学反应,质量也不会发生改变。现将含有8g氢氧化钠的水溶液109g通电一段时间后,生成1g氢气,请你计算(要有计算过程):
(1)电解所消耗的水的质量;
(2)电解水后的氢氧化钠溶液的质量分数。
【答案】(6分) (1)解:设电解所消耗的水的质量为x
2H2O![]() 2 H2↑ + O2 ↑……(1分)
2 H2↑ + O2 ↑……(1分)
36 4
x 1g ……(1分)
36﹕x=4﹕1g ……(1分)
x=9g ……(1分)
(2)电解水后的氢氧化钠溶液的溶质的质量分数为:![]() ×100%=8%……(2分)
×100%=8%……(2分)
答:略。
【解析】
(1)根据反应的化学方程式,由产生氢气的质量可计算消耗水的质量;
(2)由于反应前后氢氧化钠质量不变,改变的只是溶液中水的质量,由氢氧化钠质量与所剩余溶液的质量比,可计算电解水后的氢氧化钠溶液的质量分数.
解答:解:(1)设电解所消耗的水的质量为x
2H2O![]() 2 H2↑ + O2 ↑
2 H2↑ + O2 ↑
36 4
x 1g
![]() =
=![]()
x=9g
(2)电解水后的氢氧化钠溶液的溶质的质量分数为:
![]() ×100%=8%
×100%=8%
答:(1)电解所消耗的水的质量9g;
(2)电解水后的氢氧化钠溶液的质量分数8%.

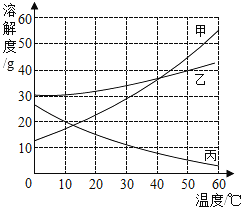
【题目】下列所示图象能正确反映对应的实验或事实的是( )
A | B | C | D | |
图象 |
|
|
|
|
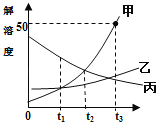
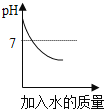
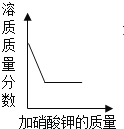
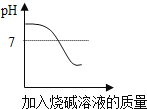
实验或事实 | 向pH等于12的氢氧化钙溶液不断加水稀释 | 20℃向一杯不饱和的KNO3溶液中逐步加入KNO3晶体 | 向稀盐酸中加入过量的烧碱溶液 | 将一定质量的碳在密闭容器中(含空气)加热 |
A. AB. BC. CD. D
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |