题目内容
【题目】青铜器浑厚凝重,繁缛富丽。

(1)青铜器的主要成分铜和锡,它们属于_____(填“金属”或“非金属”)元素。
(2)下列关于铜、锡的性质说法错误的是_____(填序号)。
A.都可以导电
B.均可以与氧气反应
C.都可以与稀盐酸反应
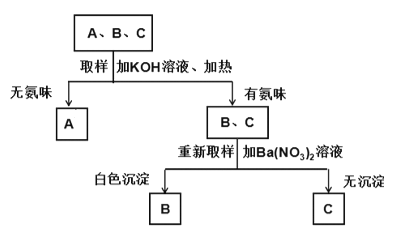
(3)一种镀锡铜线表面锡的褪除及回收的工艺流程如图所示,回答以下问题:

① Sn(OH) 4中锡(Sn)的化合价为_____,过程Ⅳ反应的基本反应类型是_____。
② 步骤Ⅲ中操作a的名称是_____。
③ 写出过程Ⅰ中发生反应的化学方程式是_____。
【答案】 金属 C +4 分解反应 过滤 Sn+CuSO4 = SnSO4+Cu
【解析】本题考查了金属的性质,化合价,反应类型以及化学方程式的书写。
(1)青铜器的主要成分铜和锡,它们属于金属元素。
(2) A、铜、锡是金属都可以导电,正确;B、铜、锡都可以与氧气反应生成氧化物,正确;C、铜在金属活动顺序中排在氢之后,不能与稀盐酸反应,错误。故选C。
(3) ① 设:Sn(OH) 4中锡(Sn)的化合价为x,根据化合价代数和为零,则有x+(-2)×2=0 x=+4,过程Ⅳ反应是Sn(OH) 4加热生成SnO2和H2O,该反应是一种物质生成两种物质,属于分解反应;
② 步骤Ⅲ中操作将固体与液体分离,操作名称是过滤;
③ 写出过程Ⅰ中发生反应是Sn与CuSO4反应生成SnSO4和Cu,化学方程式是Sn+CuSO4 = SnSO4+Cu。

【题目】安徽某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 反应后 | ||
实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
180 g | 12g | 187.6g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为___________g。
(2)求该石灰石中碳酸钙的质量分数_______________。