题目内容
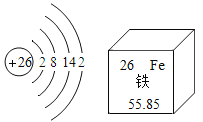
【题目】高锰酸钾在生产、生活中有广泛应用。实验小组对高锰酸钾的某些性质进行研究。
Ⅰ.不稳定性
(1)KMnO4 受热分解的化学方程式为_____,16 gKMnO4 产生 O2 的质量为_____g(列式并计算出结果)
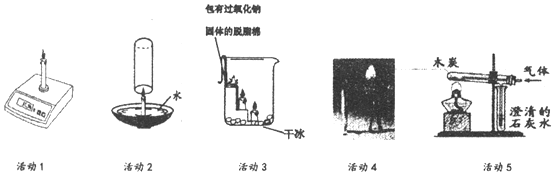
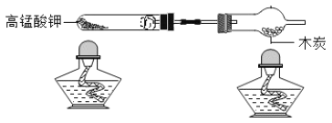
(2)将制得的氧气做如下实验:在染着的酒精灯上抖落铁粉,观察打击火星四射,如图所示。铁丝在空气中不能燃烧,铁粉却能在空气燃烧,由此说明_____。铁燃烧的化学方程式为_____。如图所示木炭遇 O2 燃烧时,现象为_____。

Ⅱ.腐蚀性
(查阅资料)KMnO4 溶液呈中性,有腐蚀性。
(进行实验)
实验 1:将新鲜鸡皮在不同浓度的 KMnO4 溶液中浸泡相同时间,现象如下表。
KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
实验 2:将铜片分别浸泡在 4 种溶液中进行实验,所得数据如下表。
编号 | ① | ② | ③ | ④ |
实验 |
25mL0.1 KMnO4 溶液 |
25mL0.1%KMnO4 溶液+10 滴浓硫酸 |
25mL 蒸馏水+ 10 滴浓硫酸 |
25 mL 1% KMnO4 溶液+10 滴浓硫酸 |
实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
18 小时后 | 0.54 | 0.52 | 0.54 | 0.43 |
(解释与结论)
(3)实验 1 的目的是_____。
(4)实验 2 中,通过对比②和④,得出的结论是_____。
(5)实验 2 中,欲得出“KMnO4 和硫酸共同作用对铜才有腐蚀性”的结论,需要对比_____(填编号)。
【答案】![]() 设16g高锰酸钾产生的氧气质量为x
设16g高锰酸钾产生的氧气质量为x
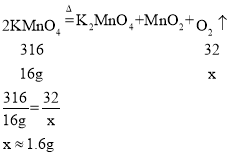
则产生氧气的质量约为1.6g 燃烧与和空气的接触面积有关 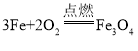 燃烧更旺,发出白光 探究不同浓度高锰酸钾对皮肤的腐蚀性 酸性环境中,高锰酸钾浓度越高,对金属的腐蚀程度越大 ①②③
燃烧更旺,发出白光 探究不同浓度高锰酸钾对皮肤的腐蚀性 酸性环境中,高锰酸钾浓度越高,对金属的腐蚀程度越大 ①②③
【解析】
(1)高锰酸钾在加热的条件下产生锰酸钾、二氧化锰和氧气,方程式为:![]() 。
。
设16g高锰酸钾产生的氧气质量为x
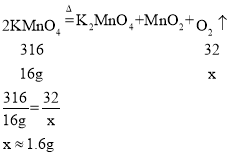
则产生氧气的质量约为1.6g
(2)铁丝在空气中不能燃烧,铁粉却能在空气燃烧,唯一的区别在于铁的状态,对比铁粉和铁丝,铁粉与空气接触更充分,由此说明燃烧与和空气的接触面积有关。铁燃烧生成火星四射,生成黑色的固体,方程式为: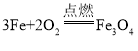 。如图所示木炭遇 O2 燃烧时,现象为燃烧更旺,发出白光。
。如图所示木炭遇 O2 燃烧时,现象为燃烧更旺,发出白光。
(3)实验 1是将新鲜鸡皮在不同浓度的 KMnO4 溶液中浸泡相同时间观察鸡皮表面的变化,将鸡皮模拟成人的皮肤,目的是探究不同浓度高锰酸钾对皮肤的腐蚀性。
(4)实验2和4唯一的不同点在于高锰酸钾溶液的浓度,实验4浓度更高,对比两实验中铜片前后质量,发现实验4变化量更大,说明酸性环境中,高锰酸钾浓度越高,对金属的腐蚀程度越大。
(5)欲得出“KMnO4 和硫酸共同作用对铜才有腐蚀性”的结论,则变量应该为有浓硫酸的高锰酸钾溶液和无浓硫酸的高锰酸钾溶液,无高锰酸钾的浓硫酸,三个实验对照,即实验①②③。

【题目】水通常是可用来灭火的,但有时水却是可引火的。同学们将少量超氧化钾(KO2)粉末用棉花包裹没有任何变化。(已知棉花和超氧化钾不反应)但如果将少量水滴到包有超氧化钾粉末的棉花上,则棉花迅速发生剧烈的燃烧(比在空气中燃烧还剧烈)。同学们对此产生好奇,在老师的指导下,完成了如下实验探究。
(提出问题)______________。
(猜想与假设)(1).超氧化钾和水反应生成___________。(2).___________。
(设计与实施)为了验证猜想,有同学提出如下实验方案:向盛有KO2的试管中滴加适量水,若看到有气泡产生,证明猜想1成立。在上述实验的试管口拴上一个气球,若气球变鼓,证明猜想2成立。你是否同意该实验方案,你的理由是____________。
在老师的指导下,同学们又进一步完善该方案并用下图所示装置进行实验验证。
实验装置 | 实验目的 | 实验操作及现象 |
| 验证猜想1 | 将带火星的木条放在_______处,发现木条复燃。 |
验证猜想2 | _______ |
(实验结论)超氧化钾与水发生的化学反应,满足了棉花燃烧的条件。