题目内容
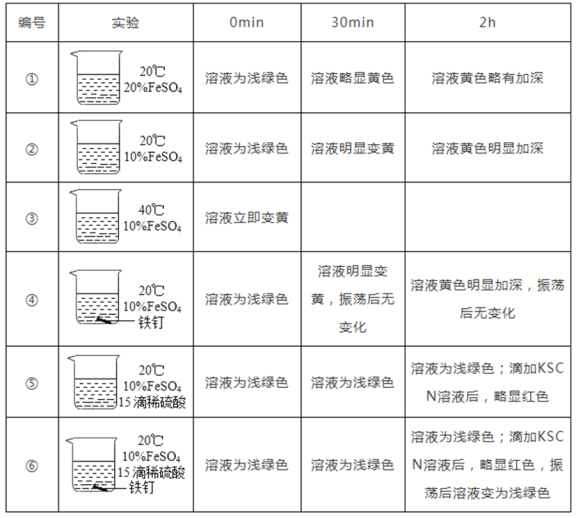
【题目】利用下图所示装置研究氧气的性质,并测定空气中氧气的含量。
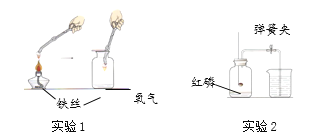
(1)实验1中观察到铁丝剧烈燃烧,火星四射,放出大量的热,_________。该反应的化学方程式为________。
(2)实验2中,点燃红磷前需要用弹簧夹夹紧胶皮管的原因是________。
【答案】生成黑色固体3Fe+ 3O2![]() Fe3O4防止红磷燃烧放热导致集气瓶中气体逸出
Fe3O4防止红磷燃烧放热导致集气瓶中气体逸出
【解析】
本题考查了空气组成的测定,氧气的化学性质。根据常见实验的现象、注意事项进行分析解答。
(1)实验1是铁丝在氧气中燃烧,观察到铁丝剧烈燃烧,火星四射,生成黑色固体,放出大量的热。铁在氧气中燃烧生成四氧化三铁,该反应的化学方程式:3Fe+ 3O2![]() Fe3O4;
Fe3O4;
(2)红磷燃烧时放出热量,气体受热膨胀。实验2中,点燃红磷前需要用弹簧夹夹紧胶皮管的原因是防止红磷燃烧放热导致集气瓶中气体逸出。

 名校课堂系列答案
名校课堂系列答案【题目】化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图)。

(猜想与假设)
小宁:可能是氢氧化钠溶液
小静:可能是(1)__________溶液
小致:可能是(2)__________溶液
小远同学认为小宁的猜想不可能,原因是(3)__________。
(实验探究)
实验操作 | 实验现象 | 结论 |
取该溶液少许,滴加(4)__________ | 有气泡产生 | (5)__________同学的猜想成立。 |
(反思与评价)
标签为什么会破损,小静同学想测定该溶液的酸碱度,她的操作步骤是:(6)__________。测得溶液的pH,(7)__________(选填>7,=7或<7),溶液显__________性(选填酸性、中性或碱性)致使标签破损。
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。

A | B |
(1)实验1中反应的化学方程式是_____。 (2)实验2中,加热液体时可观察到的现象是_____。 | (1)实验1的现象:剧烈燃烧,_____,放热,生成黑色固体。 (2)实验2中,石蕊溶液变红的原因是_____(用化学方程式表示)。 |