题目内容
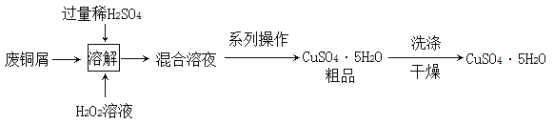
【题目】把一定质量的纯净物A和9.6gB在一定条件下按下图所示充分反应,当B消耗完时,可生成8.8gD物质和5.4gE物质。

请回答下列问题:
(1)参加反应的A物质的质量是______。
(2)请判断A物质中是否含有氧元素______。
(3)试推断A物质中各元素之间的质量比______。
【答案】4.6g 含有 12:3:8
【解析】
(1)4.6g,m(A)=8.8g+5.4g-9.6g=4.6g
(2)含有,D是CO2,CO2中m(C)=8.8g×(![]() ×100%)=2.4g
×100%)=2.4g
E是H2O,H2O中m(H)=5.4g×(![]() ×100%)=0.6g
×100%)=0.6g
2.4g+0.6g=3g<4.6g,因此A中含有氧元素。
(3)A中m(O)=4.6g-3g=1.6g,
故A中各元素的质量比为m(C):m(H):m(O)=2.4g:0.6g:1.6g=12:3:8。

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
【题目】下列实验方法能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 鉴别 | 分别点燃,并在火焰上方罩干冷烧杯 |
B | 除去 | 将混合气通入足量澄清石灰水 |
C | 检验 | 加入适量饱和氯化钙溶液 |
D | 将不饱和的氯化钠溶液变饱和溶液 | 加入少量氯化钠固体 |
A.AB.BC.CD.D