题目内容
【题目】某品牌粉笔的成分为碳酸钙、硫酸钙,可能含有少量氧化钙。取37g干燥的粉笔研磨成粉末,加入足量稀盐酸,充分反应后得到8.8g气体。将反应后的固液混合物蒸干,测得其中钙元素质量为13.5g。(说明:硫酸钙与稀盐酸不反应)
(1)根据化学方程式计算37g粉笔中碳酸钙的质量。
(2)推断该粉笔中是否含有氧化钙。
【答案】(1)20g
(2)含有氧化钙
【解析】
根据生成的二氧化碳的质量和对应的化学方程式求算碳酸钙的质量,进而结合化学式求算和分析对应的钙元素的质量分数,从而分析是否含有氧化钙。
解:
设碳酸钙的质量为x
根据题意二氧化碳只来源于碳酸钙和盐酸反应。
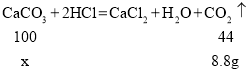
![]()
x=20g
测得其中钙元素质量为13.5g,而碳酸钙中的钙元素的质量为20g×![]() ×100%=8g,则其余物质钙元素含量为13.5g﹣8g=5.5g
×100%=8g,则其余物质钙元素含量为13.5g﹣8g=5.5g
假设全部来自硫酸钙,则对应的硫酸钙的质量为5.5g÷![]() =18.7g
=18.7g
而样品硫酸钙的质量最多可能为37g﹣20g=17g。所以一定含有氧化钙。
故答案为:
(1)20g;
(2)含有氧化钙。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目




